Acétonitrile (C2H3N)
- 894
- 182
- Raphaël Charles
Qu'est-ce que l'acétonitrile?
Il acétonitrile Il s'agit d'une substance d'origine organique composée uniquement de carbone, d'hydrogène et d'azote. Cette espèce chimique appartient au groupe de nitriles, l'acétonitrile étant la structure la plus simple parmi les types organiques.
Les nitriles sont une classe de composés chimiques dont la structure est constituée par un groupe de cyanure (CN-) et une chaîne radicale (-r). Ces éléments sont représentés par la formule générale suivante: R-C≡N.
Il est connu que cette substance est principalement originaire de la production d'une autre espèce appelée acrilonitrile (un autre nitrile simple, de formule moléculaire C3H3N, qui est utilisé dans l'élaboration des produits dans l'industrie textile) comme sous-produit du même.
De plus, l'acétonitrile est considéré comme un solvant avec des propriétés de polarité moyenne, c'est pourquoi il est utilisé assez régulièrement dans l'analyse RP-HPLC (acronyme en anglais pour la chromatographie liquide à haute efficacité de la phase inverse).
Structure
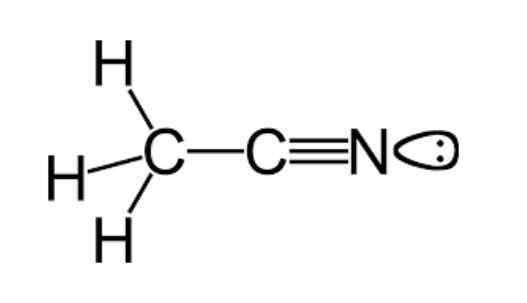
Comme mentionné précédemment, l'acétonitrile appartient au groupe fonctionnel de nitriles, ayant une formule moléculaire couramment représentée comme C2H3N, qui peut être observé dans la formule structurelle illustrée dans la figure supérieure.
Cette image montre une classe de lobe attachée à l'atome d'azote, qui représente la paire d'électrons manquants que cet atome possède, et qui lui donne une grande partie des propriétés de réactivité et de stabilité qui sont caractéristiques.
De cette façon, cette espèce manifeste un comportement très particulier en raison de son arrangement structurel, ce qui se traduit par une faiblesse pour recevoir des liaisons hydrogène et peu de capacité à donner des électrons.
Peut vous servir: Arsenic: histoire, structure, propriétés, utilisationsDe même, cette substance est née pour la première fois dans la seconde moitié des années 1840, fabriquée par le scientifique nommé Jean-Baptiste Dumas, dont la nationalité était française.
La conformation structurelle de cette substance permet cette caractéristique d'un solvant de nature organique.
À son tour, cette propriété permet à l'acétonitrile d'être mélangé avec de l'eau, en plus d'une série d'autres solvants d'origine organique, à l'exception des hydrocarbures ou des espèces d'hydrocarbures saturés.
Propriétés de acétonitrile
Ce composé a une série de propriétés qui la distinguent des autres de la même classe, qui sont répertoriées ci-dessous:
- Il est dans un état d'agrégation liquide dans des conditions de pression et de température standard (1 atm et 25 ° C).
- Sa configuration moléculaire lui donne une masse molaire ou un poids moléculaire d'environ 41 g / mol.
- Il est considéré comme le nitrile qui a la structure la plus simple, parmi les types organiques.
- Ses propriétés optiques lui permettent une incolore dans cette phase liquide et des caractéristiques limpides, en plus d'avoir une odeur aromatique.
- Il a un point d'inflammation autour de 2 ° C, équivalent à 35,6 ° F ou 275,1 K.
- Il présente un point d'ébullition dans la plage de 81,3 à 82,1 ° C, une densité d'environ 0,786 g / cm3 et un point de fusion entre -46 à -44 ° C.
- Il est moins dense que l'eau mais miscible avec cela et avec une variété de solvants organiques.
- Manifeste une constante diélectrique de 38,8 en plus d'un moment dipolaire d'environ 3,92 jours.
- Il est capable de dissoudre une grande variété de substances d'origine ionique et de nature non polaire.
- Il est tout à fait utilisé comme phase mobile dans l'analyse HPLC, qui présente des propriétés inflammabilité élevées.
Utilisations / applications
Parmi le grand nombre d'applications de l'acétonitrile, les éléments suivants peuvent être comptés:
- De même, d'autres espèces de nitriles, cela peut passer par un processus de métabolisation dans les microsomes (éléments vésiculaires qui font partie du foie), en particulier dans cet organe, pour créer de l'acide cyanridique.
- Il est utilisé de manière très généralisée comme phase mobile dans le type d'analyse appelé chromatographie liquide à phase inverse élevée élevée (RP-HPLC); c'est-à-dire que la substance éluée qui a une stabilité élevée, un grand éluant et une viscosité diminuée.
- Dans le cas des applications de magnitude industrielle, ce composé chimique est utilisé dans les raffineries de pétrole brut comme solvant dans certains processus, tels que la purification de l'alcène appelé Butadieno.
- Il est également utilisé comme ligand (espèces chimiques combinées avec un atome d'un élément métallique, considéré comme central dans la molécule donnée, pour former un composé de coordination ou un complexe) dans un grand nombre de composés de nitrile avec des métaux du groupe de transition.
- De même, il est utilisé dans la synthèse de type organique pour un grand nombre de produits chimiques aussi avantageux que l'acide α-naphtalène, le chlorhydrate de thiamine ou d'acétamidine.
Des risques
Les risques impliqués dans l'exposition à l'acétonitrile sont divers. Parmi ceux-ci, une toxicité diminuée lorsque l'exposition est pour une période de temps réduite et en faible quantité, étant métabolisée pour la production d'acide cyanhydrique.
De même, il y a eu des cas de personnes qui ont empoisonné avec cette espèce chimique, empoisonnée par le cyanure présent dans la molécule après avoir été en contact avec de l'acétonitrile à différents degrés (lors de l'inhalation, de l'ingestion ou de l'absorption à travers la peau).
Peut vous servir: huile ou éther de benzine: formule, structure, utilisationsPour cette raison, les conséquences de sa toxicité sont retardées car le corps ne métabolise pas facilement cette substance dans le cyanure, car deux à douze heures sont nécessaires pour que cela se produise.
Cependant, l'acétonitrile est facilement absorbé dans la zone des poumons et le tractus gastro-intestinal. Par la suite, sa distribution se produit tout au long de l'organisme, se produisant chez les gens et même chez les animaux et atteignant les reins et la rate.
D'un autre côté, en plus des risques d'inflammabilité qu'il présente, l'acétonitrile est un précurseur de substances toxiques telles que l'acide cyanhydrique ou formaldéhyde. Même son utilisation dans des produits appartenant à la zone cosmétique dans le domaine économique européen, en 2000,.

