Triades de Döbereiner
- 3250
- 376
- Lucas Schneider
 Tableau périodique des éléments, tous les éléments chimiques jusqu'à présent découverts sont classés. Avec licence
Tableau périodique des éléments, tous les éléments chimiques jusqu'à présent découverts sont classés. Avec licence Que sont les triades de Döbereiner?
Le Triades de Döbereiner Ils sont la première expérience où trois éléments chimiques ont été regroupés qui partagent des caractéristiques similaires, les associant à leurs poids atomiques. Font partie des 118 éléments chimiques, étant la diversité des réactions montrées et leurs composés leur apparence la plus notable.
L'idée de classer les éléments est de traiter correctement leurs propriétés chimiques sans développer un ensemble de règles et de théories pour chacun d'eux.
Sa classification périodique a donné un cadre systématique extrêmement utile pour les corréler en fonction de quelques modèles très simples et logiques.
Les éléments sont systématiquement disposés en lignes et colonnes avec des nombres atomiques croissants, et l'espace pour les nouvelles découvertes a été réservé.
En 1815, seulement une trentaine d'éléments étaient connus. Bien qu'il y ait beaucoup d'informations disponibles à ce sujet et leurs composés, il n'y avait pas d'ordre apparent.
Plusieurs tentatives ont été faites pour trouver l'ordre, cependant, c'était difficile.
Découvrir les triades de Döbereiner
Le scientifique Johann Wolfgang Döbereiner (1780-1849) a fait des résultats importants sur la régularité numérique parmi les poids atomiques des éléments. Il a été le premier à remarquer l'existence de plusieurs groupes de trois éléments, qu'il a appelés triades, qui ont montré des similitudes chimiques.
Ces éléments ont révélé une relation numérique importante, car une fois ordonné en fonction de leur poids équivalent ou atomique, le poids de l'élément central s'est avéré être la moyenne approximative des deux éléments restants de la triade.
Peut vous servir: phosphate de sodium: structure, propriétés, synthèse, utilisationsEn 1817, Döbereiner a constaté que si certains éléments étaient combinés avec de l'oxygène dans des composés binaires, une relation numérique pouvait être discernée entre les poids équivalents de ces composés.
Ainsi, lorsque le calcium, le strontium et les oxydes de baryum étaient pris en compte, le poids équivalent de l'oxyde de strontium était approximativement la moyenne de l'oxyde de calcium et de l'oxyde de baryum. On dit que les trois éléments en question, le strontium, le calcium et le barum, forment une triade.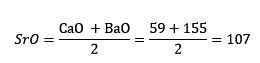
Bien que Döbereiner ait travaillé avec des pesos qui avaient été déduits de peu de méthodes expérimentales rigoureuses, mais en vigueur pour le moment, leurs valeurs sont étroitement bonnes.
L'observation de Döbereiner a eu peu d'impact sur le monde chimique, mais est devenu très influent. À l'heure actuelle, il est considéré comme l'un des pionniers du développement du système périodique.
Douze ans plus tard, en 1829, Döbereiner a ajouté trois nouvelles triades, qui sont présentées ci-dessous:
Groupe halogène
Le chlore, le brome et l'iode ont des propriétés chimiques similaires et forment une triade. Ces éléments sont des métaux très réactifs. S'ils sont répertoriés dans l'ordre de l'augmentation de la masse relative, ils sont de l'ordre de la réactivité décroissante. Bromo a une masse atomique intermédiaire entre le chlore et l'iode.

La masse atomique du brome moyen.
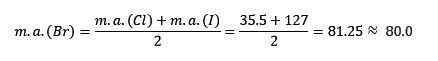
La valeur moyenne obtenue est proche de la masse atomique du brome (BR).
Similitudes dans les propriétés chimiques:
1. Ce sont tous des non-métaux.
2. Tous réagissent avec l'eau pour former des acides (par exemple, dans: HCl, HBR, HF).
Il peut vous servir: biodiesel: histoire, propriétés, types, avantages, inconvénients3. Tout le monde a une valence d'un (par exemple, dans: HCL, HBR, HF).
4. Tous réagissent avec des métaux alcalins pour former des sels neutres (par exemple, NaCl, Nabab, Nai)
Groupe de métaux alcalins
Le lithium, le sodium et le potassium ont des propriétés chimiques similaires et forment une triade. Ces éléments sont des métaux doux et légers mais très réactifs.
S'ils sont répertoriés dans l'ordre de l'augmentation de la masse atomique relative, ils sont également dans l'ordre d'augmentation de la réactivité. Le sodium a la masse atomique intermédiaire entre le lithium et le potassium.

La masse atomique de l'élément central sodium (NA) est égale à la moyenne de la masse atomique au lithium (LI) et du potassium (K).
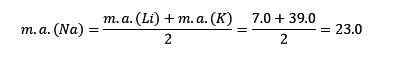
Similitudes dans les propriétés chimiques:
1. Ce sont tous des métaux.
2. Tous réagissent avec l'eau pour former des solutions alcalines et l'hydrogène gazeux.
3. Tout le monde a un Valencia de One (par exemple, dans: Licl, NaCl, KCL).
4. Ses carbonates sont résistants à la décomposition thermique.
Groupe de calcogens ou d'amphumos
Le soufre, le sélénium et le télécolaire ont des propriétés chimiques similaires et forment une triade. Le sélénium a la masse atomique intermédiaire entre le soufre et la télésure.

La masse atomique de l'élément de sélénium moyen (SE) est égale aux masses atomiques moyennes de soufre et de téléluro (TE).
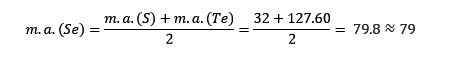
Encore une fois, la valeur moyenne obtenue est proche de la pâte atomique de sélénium (SE).
Similitudes dans les propriétés chimiques:
1. Les combinaisons avec des hydrogènes de ces éléments entraînent des gaz toxiques.
2. Chacun de ces éléments a 6 électrons de valence.
3. Les qualités métalliques augmentent à mesure que le nombre atomique augmente.
Döbereiner a également averti que pour être valide, les triades devaient révéler des relations chimiques entre les éléments, ainsi que les relations numériques.
Il peut vous servir: Chlorate de potassium (KCLO3)D'un autre côté, il a refusé de grouper le fluorure avec le chlore, le brome.
Il était également réticent à considérer l'apparition de triades entre des éléments différents, tels que l'azote, le carbone et l'oxygène, bien qu'ils aient montré une relation numérique triadique significative.
Le travail de Döbereiner s'est concentré sur les relations entre les éléments d'une triade, mais n'a donné aucune idée de la relation entre eux.
Il suffit de dire que l'enquête de Döbereiner a établi la notion de triades comme un concept puissant, que plusieurs autres produits chimiques prendraient bientôt en considération.
En fait, les triades de Döbereiner ont représenté la première étape pour regrouper les éléments en colonnes verticales dans le tableau périodique et ainsi établir un système qui explique les propriétés chimiques et révèle les relations physiques des éléments.
Expansion des triades
D'autres produits chimiques ont étendu les triades de Döbereiner pour inclure plus que les trois éléments d'origine. Par exemple, du fluorure a été ajouté au sommet de la triade contenant du chlore, du brome et de l'iode.
D'autres «triades» se sont produites, comme celle contenant de l'oxygène, du soufre, du sélénium et de la télésure. Mais il n'y avait pas de système pour les corréler comme un tout.
L'un des principaux inconvénients était que de nombreuses masses atomiques relatives étaient toujours erronées pour l'époque.
Les références
- Johann Wolfgang Döbereiner. Récupéré de Britannica.com.
- Qu'est-ce que le groupe 16 du tableau périodique? Comment ces éléments sont-ils utilisés? Récupéré de Quora.com.

