Définition de tension interfaciale, équation, unités et mesure
- 4228
- 15
- Lucas Schneider
La tension interfaciale (γ) est la force nette par unité de longueur qui est exercée sur la surface de contact entre une phase (solide ou liquide) et une autre (solide, liquide ou soda). La force nette est verticale à la surface de contact et est dirigée vers les phases.
Lorsque l'une des phases est un gaz, on l'appelle généralement tension superficielle. Les phases en contact sont non miscibles, c'est-à-dire qu'ils ne peuvent pas se dissoudre les uns avec les autres pour former une solution. La région de contact entre les phases est une surface de séparation géométrique Interface. La tension interfaciale est due aux forces intermoléculaires présentes à l'interface.
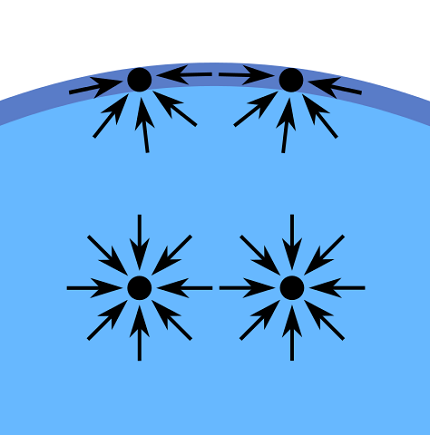
 Forces entre molécules d'un liquide en contact avec l'air [par Booyabazooka (https: // communes.Wikimedia.Org / wiki / fichier: wassermolek% c3% bcleint% c3% b6pfchen.Svg)]
Forces entre molécules d'un liquide en contact avec l'air [par Booyabazooka (https: // communes.Wikimedia.Org / wiki / fichier: wassermolek% c3% bcleint% c3% b6pfchen.Svg)] La tension interfaciale joue un rôle important dans de nombreux phénomènes interfaciaux et des processus tels que les émulsions et la production d'huile.
[TOC]
Définition
Les propriétés d'interface ne sont pas égales aux propriétés à l'intérieur des phases en contact, car différentes interactions moléculaires se manifestent car dans cette région, il existe des molécules qui appartiennent à une phase et à l'autre.
Les molécules à l'intérieur d'une phase interagissent avec les molécules voisines, qui ont des propriétés similaires. Par conséquent, la force nette intérieure est vide car les interactions attrayantes et répulsives sont égales dans toutes les directions possibles.
Les molécules qui sont à la surface entre les deux phases sont entourées de molécules de la même phase mais aussi de molécules voisines de l'autre phase.
Dans ce cas, la force nette n'est pas nulle et est dirigée vers la phase dans laquelle il y a une plus grande interaction. Le résultat est que l'état énergétique des molécules à la surface est supérieur à l'état de l'énergie dans la phase.
Peut vous servir: photo parabolique: caractéristiques, formules et équations, exemplesLa force nette qui agit vers l'intérieur par unité de longueur le long de l'interface est la tension interfaciale. En raison de cette force, les molécules ont tendance à minimiser l'énergie en minimisant la surface pour chaque unité de volume.
Définition basée sur le travail et l'énergie
Pour attirer une molécule de l'intérieur à la surface, il est nécessaire que les forces agissant sur la molécule vont surmonter la force nette. En d'autres termes, un travail est nécessaire pour augmenter la surface interfaciale.
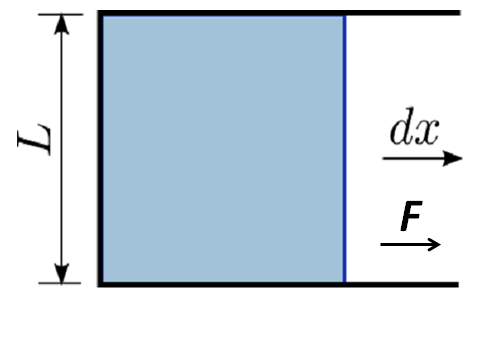 Force nécessaire pour augmenter la région interfaciale. (https: // communes.Wikimedia.org / wiki / fichier: Surface_growing.Png)
Force nécessaire pour augmenter la région interfaciale. (https: // communes.Wikimedia.org / wiki / fichier: Surface_growing.Png) Plus la force intermoléculaire est grande est grande à faire et plus l'entrée d'énergie est grande. Pour cette raison, la tension interfaciale est également définie en fonction du travail ou basé sur l'énergie, comme mentionné ci-dessous:
La tension interfaciale est le travail nécessaire pour créer une unité de zone à l'interface. De même, la tension interfaciale est définie comme l'énergie libre requise par unité de zone créée.
Équation et unités de tension interfaciale
L'équation de la tension interfaciale en fonction de la force nette intermoléculaire est:
γ = F / 2L [1]
F = Force nette
l = longueur d'interface
Le numéro 2 qui apparaît dans l'équation [1] signifie qu'il y a deux surfaces, une pour chaque face de l'interface.
La tension interfaciale en fonction des travaux nécessaires pour générer une unité de surface est exprimé par l'équation suivante:
γ = W / Δa [2]
W = Travailler
ΔA = Augmentation de la surface
La création de la zone interfaciale s'accompagne d'une augmentation de la formation de l'énergie libre.
γ = ΔE/ /ΔA [3]
ΔE = Énergie de formation d'interface
Il peut vous servir: courbe de chauffage: qu'est-ce que c'est, comment c'est fait, des exemplesLes unités de tension interfaciale du système international sont N / M ou Joules / M2. Il est également généralement utilisé dynas / cm ou mn / m.
Dépendance à la température
L'un des principaux facteurs qui affectent la tension interfaciale est la température. À mesure que la température augmente les forces d'interaction diminue, en conséquence, la force nette qui contracte la surface diminue également, provoquant une diminution de la tension interfaciale.
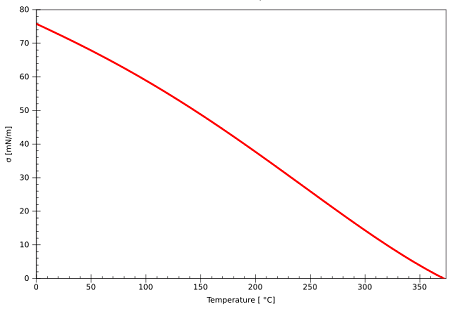 Tension de surface en fonction de la température de l'eau-aérienne [(https: // communes.Wikimedia.org / wiki / fichier: température_dependence_surface_tenion_of_water.Svg)]
Tension de surface en fonction de la température de l'eau-aérienne [(https: // communes.Wikimedia.org / wiki / fichier: température_dependence_surface_tenion_of_water.Svg)] Si la température augmente toujours, il y aura un moment où la tension interfaciale sera annulée et il n'y aura pas de surface de séparation entre les phases. La température à laquelle la tension interfaciale est annulée est appelée température critique (tc).
La raison pour laquelle la tension interfaciale diminue est que lorsque la température augmente l'énergie cinétique en raison de l'augmentation du mouvement thermique des molécules.
Mesure de la tension interfaciale
Il existe différentes méthodes de mesure expérimentale de la tension interfaciale, parmi lesquelles les plus appropriées selon les propriétés caractéristiques des phases en contact et en conditions expérimentales peuvent être choisies.
Parmi ces méthodes figurent la méthode de la plaque Wilhelmy, la méthode du anneau du Nouy, la méthode de chute en attente et la méthode de chute rotative.
Méthode de la plaque Wilhelmy
Il consiste à mesurer la force vers le bas qui exerce la surface d'une phase liquide sur une plaque en aluminium ou en verre. La force nette exercée sur la plaque est égale au poids plus la force de tension. Le poids de la plaque est obtenu par des moyens.
Méthode de l'anneau du Nouy
Dans cette méthode, la force est mesurée pour séparer la surface d'un anneau métallique d'une surface liquide garantissant qu'avant la mesure, l'anneau est complètement immergé dans le liquide. La force de séparation est égale à la tension interfaciale et est mesurée à l'aide d'un solde de haute précision.
Peut vous servir: Planck constante: formules, valeurs et exercicesMéthode de chute en attente
Cette méthode est basée sur la mesure de la déformation d'une goutte suspendue à un capillaire. La goutte est maintenue en équilibre pendant la suspension car la force de tension est égale au poids de la goutte.
L'allongement de la goutte est proportionnel au poids de la goutte. La méthode est basée sur la détermination de la longueur de la longueur de la goutte en raison de son poids.
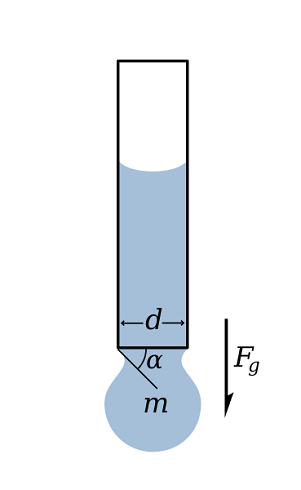 Méthode de chute de pente [par urocyon (https: // communes.Wikimedia.org / wiki / fichier: pendant_drop_test.Svg)]
Méthode de chute de pente [par urocyon (https: // communes.Wikimedia.org / wiki / fichier: pendant_drop_test.Svg)] Méthode de chute rotative
La méthode de chute rotative est très utile pour mesurer des tensions interfaciales très faibles qui s'appliquent au processus de production d'émulsions et de microémulsions.
Il consiste à placer une goutte d'un liquide moins dense à l'intérieur d'un tube capillaire plein d'un autre liquide. La goutte est soumise à une force centrifuge due à un mouvement de rotation, avec une grande vitesse, qui allonge la goutte sur l'axe y et s'oppose à la force de tension.
La tension interfaciale est obtenue à partir des dimensions de la forme géométrique de la goutte, déformée et de la vitesse de rotation.
Les références
- Tadros, t f. Appliquer des tensioactifs. Berkshire, Royaume-Uni: Wiley-VCH Verlag GmbH & Co, 2005.
- Van Oss, C J. Forces interfaciales dans les médias aqueux. Floride, États-Unis: Taylor & Francis Group, 2006.
- Figure, L et Teixeira, A A. Physique alimentaire: Propriétés physiques - Mesure et applications. Allemagne: Springer, 2007.
- Anton de Salager, R E. Tension interfaciale. Mérida: Firp - Universidad de Los Andes, 2005.
- Speight, J G. Handbook of Petroleum Product Analysis. New Jersey, États-Unis: Jhon Wiley & Sons, 2015.
- Adamson, W et Gast, un P. Chimie physique des surfaces . États-Unis: John Wiley & Sons, Inc. , 1997.
- Blunt, M J. Débit multiphase en moyenne perméable: une perspective à l'échelle des pores. Cambridge, Royaume-Uni: Cambridge University Press, 2017.
- « Caractéristiques, structures et fonctions de la polymérase
- 10 douanes de la région des Caraïbes en Colombie »

