Solutions d'amortisseur

- 3689
- 973
- Anaïs Julien
Nous expliquons quelles sont les solutions d'amortissement, leurs propriétés, composants, types et donnent plusieurs exemples
 Les solutions d'absorption des chocs régulent le pH autour d'une valeur spécifique
Les solutions d'absorption des chocs régulent le pH autour d'une valeur spécifique Quelles sont les solutions d'amortissement?
Le solutions d'amortisseur, Des solutions aqueuses formées par l'acide faible et sa base conjuguée ou une base faible et son acide conjugué.
Ils sont appelés solutions d'amortisseur, car ils ont la capacité de amortir le changement de pH après l'ajout d'acides ou de bases en petites quantités, même si ce sont des acides ou des bases forts.
Les solutions d'amortisseur sont très utiles, car elles permettent au pH d'être constant. Il existe de nombreuses réactions chimiques qui ont besoin d'un pH spécifique et constant pour bien fonctionner.
Propriétés des solutions morpainaires
Ce sont des solutions aqueuses
Le concept de pH et l'échelle de pH n'ont du sens que dans les solutions aqueuses, donc tous les tampons ou solutions d'amortissement sont préparés dans l'eau.
Son opération est basée sur l'équilibre acide-base et les principes du chatlier
Les tampons sont basés sur des réactions de dissociation acide / base réversibles qui sont en équilibre. En ajoutant des acides ou des bases forts à l'environnement, cet équilibre est perturbé, donc le système réagit pour contrer la perturbation, en suivant les principes du catelier. C'est ainsi que les tampons parviennent à amortir les grands changements du pH.
Votre pH est facilement calculé avec l'équation de Henderson-Haselbalch
Quel que soit le type de solution d'absorbeur, son pH avant et après avoir ajouté de petites quantités d'acides ou de bases forts, il peut être calculé au moyen de l'équation de Henderson-Hohaselbalch:
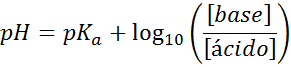
Où [la base] fait référence à la concentration molaire de la base (ou du sel de la base conjuguée) et [l'acide] fait référence à la concentration molaire de l'acide (ou du sel de l'acide conjugué).
Peut vous servir: matériaux élastiquesIls sont capables de neutraliser partiellement les acides et les bases
Les solutions d'amortissement sont constituées d'une substance de base et d'une substance acide, qui peut neutraliser les bases et les acides, respectivement. Pour cette raison, ils peuvent amortir le pH après l'ajout à la fois des acides forts et des bases fortes.
Son fonctionnement dépend de la température
Le pH d'une solution tampon dépend de l'acidité ou de la constante de base de l'acide ou de la base faible qu'il contient. Cette constante dépend de la température, donc le fonctionnement de ces solutions dépend également de la température.
Plus sa capacité est concentrée, plus sa capacité à amortir ou à réguler le pH
La capacité d'amortissement dépend de la concentration totale de la solution est supérieure à la concentration finale de l'acide ou de la base forte qui est ajoutée. Pour cette raison, plus la concentration totale de la solution tampon est grande, plus sa capacité à amortir des acides ou des bases fortes.
Composants d'une solution d'amortissement ou de tampon
Chimiquement, des solutions d'amortissement ne sont formées que par deux composants. Ces composants peuvent être un acide faible mélangé à un sel de sa base conjuguée ou une base faible mélangée à un sel de son acide conjugué.
Il existe deux façons différentes d'obtenir ces composants dans la même solution, comme nous le verrons ci-dessous:
1. Préparation de tampons de mélange de solutions de ses composants
C'est le moyen le plus direct de préparer une solution tampon. Pour ce faire, des solutions séparées d'acide faible (par exemple, de l'acide acétique) et un sel de base conjugué (par exemple, de l'acétate de sodium) sont préparés des solutions séparées). Ensuite, les deux solutions se mélangent progressivement jusqu'au pH souhaité.
Il peut vous servir: ion ammonium (NH4 +): formule, propriétés et utilisations
- Les solutions sont mixtes peu à petit jusqu'à ce que le pH souhaité
2. Préparation de tampons par neutralisation partielle d'une solution d'un acide faible
Dans ce cas, une solution d'acide faible est préparée avec la concentration totale souhaitée, puis l'hydroxyde de sodium ou de potassium est ajouté peu à petit jusqu'à atteindre le pH souhaité.
Types de solutions tampons
Les solutions d'amortisseur peuvent être classées en fonction des types de composants qu'ils possèdent ou en fonction de leur pH final.
Selon les types de composants:
- Tampon de base faible et conjugué: Dans ces cas, le pH dépend de PKpour d'acide faible.
- Tampon de base faible et acide conjugué: Dans ces cas, le pH dépend de PKb faible.
- Tampon de sels d'acide polyprotique: Dans certains cas, le rôle de l'acide faible et sa base conjuguée sont tous deux des sels de la neutralisation partielle d'un acide qui a plusieurs protons tels que l'acide sulfurique ou la phosphorique.
Selon son pH final:
Selon l'acidité ou la constante de base, une solution tampon peut réguler le pH autour de différentes gammes de pH, donnant naissance à trois types de tampons:
- Tampons d'acide: Sont ceux qui régulent le pH autour des valeurs inférieures à 7. Ils sont préparés avec des acides faibles dont PKpour être moins de 7 ou avec des bases faibles dont le pkb être supérieur à 7.
- Tampons neutres: Sont ceux qui régulent le pH autour de 7. Ils sont généralement constitués d'acides ou de bases faibles qui ont un PKpour ou un pkb près de 7.
- Tampons alcalins: Sont ceux qui régulent le pH autour des valeurs supérieures à 7. Ils sont préparés avec des acides faibles dont PKpour être supérieur à 7 ou avec des bases faibles dont le pkb est moins de 7.
Exemples de tampons ou de solutions d'amortissement
Tampon d'acide acétique / acétate de sodium
Il s'agit d'un tampon d'un acide faible (acide acétique) et d'un sel de sa base conjuguée (acétate de sodium). L'équilibre impliqué et sa constante d'équilibre sont:
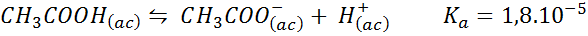
Ce tampon régule le pH autour 4.74.
Tampon d'ammoniac / chlorure d'ammonium
Il s'agit d'un tampon de base faible (ammoniac ou hydroxyde d'ammonium) et un sel de son acide conjugué (chlorure d'ammonium). L'équilibre impliqué et sa constante d'équilibre sont:
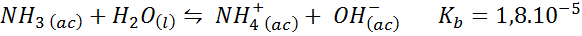
Il s'agit d'un tampon alcalin qui régule le pH autour 9.26.
Tampon de bisulfate / sulfate
Dans ce cas, l'ion bisulfate joue le papier de l'acide faible dont la base conjuguée est l'ion sulfate. L'équilibre impliqué est:
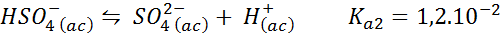
Il s'agit d'une solution de dommage acide qui régule le pH autour 3.05.
Tampon d'acide carbonique / bicarbonate
C'est l'un des systèmes de régulation de pH les plus importants de notre sang. La réaction impliquée est: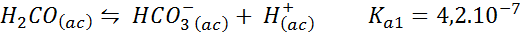
Ce tampon régule le pH autour 6.38.
Tampon dihydrogène phosphate / phosphate d'hydrogène
C'est l'un des systèmes de régulation de pH les plus utilisés en biologie et biochimie, car il permet de réguler le pH très proche du pH physiologique auquel la plupart des réactions chimiques dans les cellules se produisent. La réaction est:
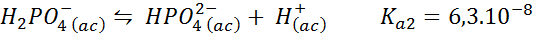
Ce tampon régule le pH autour 7.20.

