Structure promise (PM), propriétés, obtention, utilisations

- 1891
- 154
- Justine Charpentier
Il promis C'est un élément chimique qui appartient à la classe Lantanids. Il est identifié avec le symbole PM et son numéro atomique est 61. C'est un solide métallique radioactif et est l'élément le plus instable des 84 premiers éléments du tableau périodique.
Cet élément se trouve naturellement à de très faibles concentrations (environ 4 x 10-quinze grammes par kg) dans un type d'uraninite, qui est un minéral d'uranium, dans lequel la promise est présente en raison de la fission spontanée de l'uranium-238.
 Symbole, nombre atomique et masse atomique de la promesse. Source: ME / CC BY-S (https: // CreativeCommons.Org / licences / by-sa / 2.5). Source: Wikimedia Commons.
Symbole, nombre atomique et masse atomique de la promesse. Source: ME / CC BY-S (https: // CreativeCommons.Org / licences / by-sa / 2.5). Source: Wikimedia Commons. A pesar de su escasez en la corteza terrestre, ha sido detectado en el espectro de la estrella HR465 de la constelación Andrómeda, sobre cuya superficie se estima que se ha estado formando recientemente, pues ningún isótopo de Pm tiene una vida media más larga de 17 ,7 ans.
Il était utile dans des objets qui brillent dans le noir, mais en raison de leur radioactivité, il a cessé de l'utiliser dans ces. Il est utilisé pour mesurer les épaisseurs de matériau et les batteries d'énergie nucléaire.
[TOC]
Découverte
L'existence du Prometio a été soupçonnée en 1902 par le chimiste tchèque Bohuslav Brauner. Plus tard, en 1914, le physicien anglais Henry Moseley a découvert dans ses études qu'un élément manquait entre le néodyme et le Samarium.
Par la suite, bien que plusieurs groupes de chercheurs (Italiens en 1924, les Américains en 1926 et 1938) ont annoncé leur découverte, la difficulté de la séparer des autres éléments et de reproduire les expériences n'a pas pu être en mesure de prendre du mérite.
 Jacob A. Marinsky. Domaine ORNL / Pub. Source: Wikimedia Commons.
Jacob A. Marinsky. Domaine ORNL / Pub. Source: Wikimedia Commons. Enfin, en 1944, les chercheurs Marinsky J.POUR., Glendenin L.ET. et Coryell C.D. Ils ont testé leur présence et l'ont isolé des produits de la fission d'uranium dans le réacteur nucléaire des laboratoires Clinton à Oak Ridge au Tennessee, États-Unis.
 Larry E. Glendenin. Domaine ORNL / Pub. Source: Wikimedia Commons.
Larry E. Glendenin. Domaine ORNL / Pub. Source: Wikimedia Commons. Cependant, ils n'ont revendiqué la priorité dans la découverte qu'en 1946 pour avoir été pleinement consacrée aux enquêtes secrètes liées aux activités de défense pendant la Seconde Guerre mondiale.
Affectation de nom
Bien que les chercheurs aient proposé de l'appeler "Clintonium" en l'honneur des laboratoires où ils travaillaient, la femme de Coryell les a convaincus de l'appeler "promis" comme un souvenir du Titan grec Prometheus ou de Prometheus.
 Charles D. Coryell. Auteur de la photo: Christian A. Coryell / gfdl (http: // www.gnou.Org / copyleft / fdl.html). Source: Wikimedia Commons.
Charles D. Coryell. Auteur de la photo: Christian A. Coryell / gfdl (http: // www.gnou.Org / copyleft / fdl.html). Source: Wikimedia Commons. Selon certaines interprétations de la mythologie grecque, Prométhée a volé le feu des dieux pour le donner à l'humanité, il a donc été cruellement puni pour toute l'éternité. D'autres légendes disent qu'elle a fourni des êtres humains en mathématiques, des sciences, de l'agriculture et de la médecine, et même de l'homme créé.
Il peut vous servir: Clausius-Clapeyron Equation: à quoi sert, des exemples, des exercices Représentation de Prométhée par un sculpteur allemand. © El Grafo / cc-by-sa-4.Domaine 0 / pub. Source: Wikimedia Commons.
Représentation de Prométhée par un sculpteur allemand. © El Grafo / cc-by-sa-4.Domaine 0 / pub. Source: Wikimedia Commons. Ces doutes sur ce qui a été la contribution de Prométhée à l'humanité ressemble à l'incertitude quant à qui a découvert l'élément. D'un autre côté, selon l'épouse de Coryell, le nom a été justifié car les chercheurs avaient "volé le feu des dieux" lors de la découverte pendant le programme secret de la bombe atomique.
Structure électronique
La configuration électronique de cet élément est:
1s2; 2s2 2p6; 3s2 3p6 3ddix; 4s2 4p6 4ddix; 5s2 5p6; 4F5 6s2;
qui peut également être exprimé comme:
[Xe] 4F5 6s2.
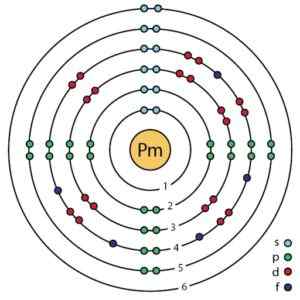 Structure électronique de Prometio selon le modèle atomique amélioré de Bohr. Ahazard.ScienceWriter / CC BY-SA (https: // CreativeCommons.Org / licences / by-sa / 4.0). Source: Wikimedia Commons.
Structure électronique de Prometio selon le modèle atomique amélioré de Bohr. Ahazard.ScienceWriter / CC BY-SA (https: // CreativeCommons.Org / licences / by-sa / 4.0). Source: Wikimedia Commons. Nomenclature
- Symbole promis, PM.
- ProMetio-147, PM-147 ou 147PM: Isotope del Prometio avec masse atomique 147.
Propriétés du prometio
État physique
Solide métallique situlé, cristaux hexagonaux.
Masse atomique
144.91
Point de fusion
1042 ºC
Point d'ébullition
3000 ºC
Densité
7,26 g / cm3
Propriétés chimiques
Il appartient à la famille des lantanides, des lantanoïdes ou des "terres rares", appelées parce que dans la croûte terrestre, elles sont toujours sous la forme de leurs oxydes. Font partie de la période 6 du tableau périodique des éléments.
Selon les sources consultées, le PM, comme les autres lantanidés, réagit directement avec l'eau, lentement froide, rapidement lors du chauffage, libérant de l'hydrogène (H2). Il s'assombrit rapidement dans l'air et brûle facilement son oxyde.
Plus de 30 composés Prometio ont été préparés et le plus présente un certain type de coloration. Son statut d'oxydation dans ces composés est +3. Ne forme pas les cations tétravalents.
Formation de certains composés
En le dissolvant dans l'acide chlorhydrique (HCl) Le promis forme le PMCL3 qui est jaune et soluble dans l'eau. Dans l'acide nitrique (HNO3) PM est généré (non3)3 qui est rose et aussi soluble dans l'eau.
Si une solution contenant des ions PM3+ est alcalisé avec NH3, C'est-à-dire que le pH est augmenté, l'hydroxyde précipite (PM (OH)3) brun clair.
Peut vous servir: lien ionique: caractéristiques, comment elle est formée et des exemplesSulfate PM2(SW4)3 Il est légèrement soluble dans l'eau. Si l'oxalate de Prometio est chauffé, il devient l'oxyde PM2SOIT3 blanc ou lavande.
Émission radioactive
Émet un rayonnement bêta sous forme d'électrons qui quittent le noyau de leurs atomes. Lorsque vous l'émettez, il devient l'élément samarium (SM). D'un autre côté, il peut devenir néodyme (ND) en éliminant un positron de base et la capture d'un électron dans le même. Le PM n'émet pas les rayons gamma.
Isotopes
Jusqu'à présent, 14 isotopes de ProMetio sont connus, avec des masses atomiques qui varient de 134 à 155. Tous sont instables (radioactifs), qui le différencie des autres lantanides.
Le ProMetio-147 est celui qui a le plus grand service public et a une demi-vie de 2,6 ans.
Isotope avec une plus grande demi-vie
L'isotope la plus longue de la demi-vie est le prométio-145 avec 17,7 ans, qui se désintègre par capture électronique, qui se compose d'un électron atomique est combiné avec un proton et forme un neutron et un neutrino.
Cependant, c'est le seul isotope de PM qui peut également souffrir de désintégration alpha (émission de 2 neutrons). En effet. Mais c'est un type de décroissance qui se produit très peu.
Courant l'obtention
En 1963, environ 10 grammes de prométio ont été préparés à l'aide de méthodes de chromatographie d'échange d'ions dans les déchets de carburant du réacteur atomique. Aujourd'hui, il se rétablit toujours de cette manière en tant que sels de 147P.m3+.
Selon certaines sources, il a également été préparé au cours de ces années par réduction du fluor (PMF3) Avec du lithium vapeur (li). Il est également préparé par réduction du chlorure (PMCL3) Avec du calcium (CA) à des températures élevées.
Il peut également être obtenu à partir du néodyme-146. Cet isotope est soumis à un bombardement avec des neutrons afin que chaque atome capture un neutron et devient néodyme-147. Ce dernier prend environ 11 jours souffrant de désintégration bêta, se transformant ainsi dans le ProMetio-147.
Applications
L'isotope 147 (147Pm) est celui qui a été le plus utilisé, étant le seul à trouver commercialement. N'émet pas les rayons gamma et est fourni sous forme d'oxyde ou de chlorure. Cependant, leur transport et leur manipulation nécessitent une protection contre les radiations.
Il peut vous servir: hydrolyse: qu'est-ce que c'est et des exemples de réactionsIl possédait certaines utilisations que aujourd'hui ne l'a plus, car elle est actuellement utilisée dans des applications spéciales.
Dans les batteries
ProMetio-147 est utilisé dans les batteries atomiques à long terme. Dans ce cas, de petits morceaux du PM sont placés dans la matrice d'un semi-conducteur pour convertir les émissions bêta en électricité.
Ce type de batteries d'énergie nucléaire peut fournir de l'énergie pendant environ 5 ans et a été utilisé dans tous les types d'appareils, des missiles aux stimulateurs cardiaques, qui sont des appareils placés chez les patients souffrant de problèmes cardiaques.
 Les stimulateurs peuvent avoir des batteries longues à base de prometio. Auteur: 242799. Source: Pixabay.
Les stimulateurs peuvent avoir des batteries longues à base de prometio. Auteur: 242799. Source: Pixabay. Dans les applications médicales
Selon certaines sources, l'oxyde de Prometio est utilisé en médecine comme source de rayonnement.
Dans l'industrie
Il a été utilisé pour mesurer l'épaisseur de certains matériaux, ce qui se fait en mesurant le rayonnement bêta qui traverse les échantillons.
Applications potentielles
Il pourrait être utilisé comme source de rayons X transportable, mais apparemment, cette application n'a pas encore été développée commercialement.
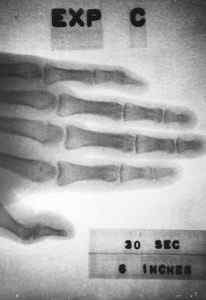 Image à rayons X obtenue en 1963 avec un petit appareil (environ 10 cm x 5 cm x 1 cm) contenant du prometio-147. Énergie.Domaine Gov / Pub. Source: Wikimedia Commons.
Image à rayons X obtenue en 1963 avec un petit appareil (environ 10 cm x 5 cm x 1 cm) contenant du prometio-147. Énergie.Domaine Gov / Pub. Source: Wikimedia Commons. Il servirait également à fournir de l'énergie à l'espace et aux sondes satellites ou à créer des appareils qui permettent la communication avec les sous-marins.
Utilisation abandonnée dans les signaux légers
Initialement, le ProMetio-147 a été utilisé pour remplacer l'élément radio dans les cadrans lumineux, car on a appris que la radio était trop dangereuse. Pour cela, le PMCL était mélangé3 Avec des luminophores, qui brillent du jaune verdâtre au bleu lorsque le rayonnement des (particules bêta) promis les a un impact.
 Il y a quelques dizaines d'années, les aiguilles des montres de bracelet ont pu être vues dans l'obscurité en raison de la luminosité causée par la radioactivité du prometio. Auteur: Monacocannes. Source: Pixabay.
Il y a quelques dizaines d'années, les aiguilles des montres de bracelet ont pu être vues dans l'obscurité en raison de la luminosité causée par la radioactivité du prometio. Auteur: Monacocannes. Source: Pixabay. Cette propriété a été utilisée dans des montres ou des cadrans de bracelet pour briller dans l'obscurité. Également dans le bouton d'allumage de certaines lampes fluorescentes. De plus, il n'a pas endommagé les luminophores comme c'est le cas avec d'autres sources de rayonnement bêta, prolongeant la durée de vie des appareils.
Cependant, lorsqu'il a été découvert que la promesse est également dangereuse, son utilisation sur le marché des objets qui brillent dans l'obscurité.
Des risques
Le PM est un élément radioactif, il doit donc être manipulé avec une extrême prudence et avec une protection raisonnable. En plus des particules bêta qu'elle émet, celles-ci peuvent avoir un impact sur les éléments avec un nombre atomique majeur et générer des rayons X.
 Les échantillons de Prometio doivent être transportés dans un bouclier de plomb épais pour éviter les effets nocifs du rayonnement qu'ils émettent. Énergie.Domaine Gov / Pub. Source: Wikimedia Commons.
Les échantillons de Prometio doivent être transportés dans un bouclier de plomb épais pour éviter les effets nocifs du rayonnement qu'ils émettent. Énergie.Domaine Gov / Pub. Source: Wikimedia Commons. Les références
- OU.S. Bibliothèque nationale de médecine. (2019). Prométhium - PM (élément). Récupéré de pubchem.NCBI.NLM.NIH.Gouvernement.
- Ganjali, m.R. et al. (2016). Introduction à la série Lanthanide (de Lanthanum à Lotetium). Prométhium. Dans la détermination de la série Lanthanides par diverses méthodes analytiques. Récupéré de ScienceDirect.com.
- Choppin, g. et al. (2013). L'origine de l'univers et de la nucléosynthèse. Capture de neutrons lents. En radiochimie et chimie nucléaire (quatrième édition). Récupéré de ScienceDirect.com.
- Diriger, D.R. (éditeur) (2003). CRC Handbook of Chemistry and Physics. 85e CRC Press.
- Coton, F. Albert et Wilkinson, Geoffrey. (1980). Chimie inorganique avancée. Quatrième édition. John Wiley & Sons.
- Société royale de chimie. (2020). Prométhium. RSC a récupéré.org.
- « Types de variables de recherche, caractéristiques et exemples
- Méthodes de séparation des mélanges homogènes »

