Méthodes et caractéristiques de séparation du mélange

- 824
- 4
- Noa Da silva
Les Méthodes de séparation du mélange Ce sont les procédures qui permettent d'obtenir une ou plusieurs composantes d'un mélange sans modifier ses propriétés chimiques. Par conséquent, il est dit qu'ils sont basés sur des techniques purement physiques, étrangères aux réactions chimiques ou à l'utilisation de substances corrosives.
Ces méthodes font partie de notre quotidien, soit dans un travail sur le terrain ouvert, soit dans les espaces de cuisine ou dans une entreprise. Ils s'appliquent dans le but de purifier ou d'augmenter la qualité d'un produit. Par exemple, le café filtre pour récupérer le précieux liquide sans interférer avec les grains moulus dans le palais.
 La coulée de café est la méthode de séparation la plus utilisée lors de la préparation du café artisanal. Source: Pexels.
La coulée de café est la méthode de séparation la plus utilisée lors de la préparation du café artisanal. Source: Pexels. Dans ce cas, c'est un mélange liquide-solide, où le liquide est du café, et le solide les grains moulus. À son tour, le café lui-même est un autre mélange: un produit de solution d'une extraction, qui est homogène.
Ainsi, il y a des mélanges hétérogènes et homogènes. Chacun d'eux a ses propres méthodes de séparation, capables d'isoler leurs composants respectifs. Comment se reconnaître? Pour la présence de plus d'une phase matérielle. Cela signifie qu'il doit y avoir deux composants parfaitement différenciables à l'œil nu.
Le café servi est un mélange homogène, car là où son apparence est examinée, c'est liquide. Au lieu de cela, un verre avec de l'eau et des graines de lin est un mélange hétérogène: l'eau liquide est une phase matérielle, tandis que les graines correspondent à une autre.
En termes généraux, les méthodes de séparation des mélanges hétérogènes nécessitent plus de travail mécanique. Pour les mélanges homogènes, en attendant, ils ont besoin d'une aide à la température. Par exemple, l'évaporation est la méthode la plus couramment utilisée pour séparer le soluté de solvant dans les solutions.
[TOC]
Principales méthodes de séparation des mélanges
- Filtration
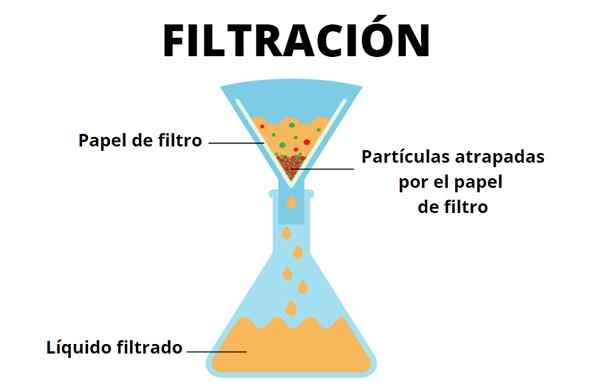
La filtration est une méthode de séparation utilisée pour séparer, en principe, les mélanges liquides solides. Vous avez besoin de l'aide d'une barrière ou d'un filtre qui permet le passage du liquide, mais qui conserve votre tissu solide, qui ne peut pas traverser les minuscules pores du filtre.
Normalement, la filtration est assistée par la gravité, et en fonction de la taille des particules solides, cela peut être un processus lent ou rapide.
Le mot «filtration» est également utilisé lorsque vous parlez d'air. Par exemple, un air contaminé par des bactéries est un mélange gazeux et homogène. Si l'air passe par des filtres qui capturent les bactéries, on dit que l'air a fui. De cette façon, il est assuré qu'il est propre et stérile.
Il peut vous servir: acide perchlorique: formule, caractéristiques et utilisationsL'eau filtrée est obtenue grâce au fait que ses impuretés et ses sédiments sont conservés par des filtres spéciaux.
Dans les laboratoires, c'est là que l'utilisation de cette méthode est la plus observée. Presque toujours après avoir obtenu un précipité ou des cristaux, ils se filtrent immédiatement pour se débarrasser du liquide et garder le solide.
- Décantation
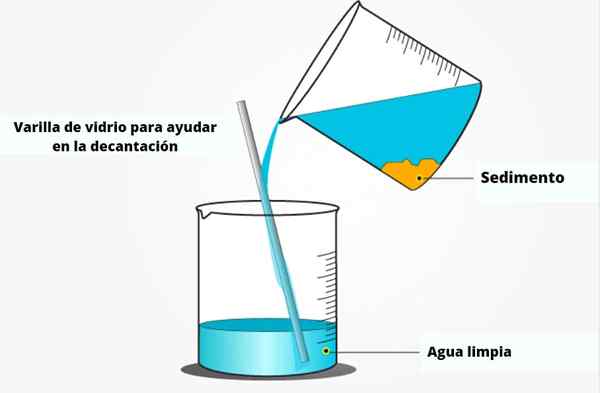 Processus de décantation pour séparer un mélange hétérogène solide
Processus de décantation pour séparer un mélange hétérogène solide La décantation maintient une certaine similitude avec la filtration. Il sert également à séparer les mélanges liquides solides, avec la différence que vous n'avez pas besoin de filtre, papier, tamis, maillage, etc., qui empêchent le passage de solide. Pour rendre cela possible, il doit y avoir une sédimentation ferme; c'est-à-dire que les sédiments doivent être soumis aux murs internes du récipient.
Par exemple, la décantation est utilisée si vous souhaitez séparer un mélange d'eau avec du sable ou des sédiments. Comme? Inclinant le verre à un autre récipient pour que l'eau, par action de gravité, tombe sans traîner le sable ou les sédiments.

Une autre différence de la décantation de la filtration est que la décantation peut être appliquée pour également séparer les mélanges liquides-liquides. Ceux-ci ne se déroulent que lorsque les deux liquides sont non miscibles, formant deux phases reconnaissables. Les mélanges pétroliers ou hydrofuleux sont des exemples de ce type de mélanges.
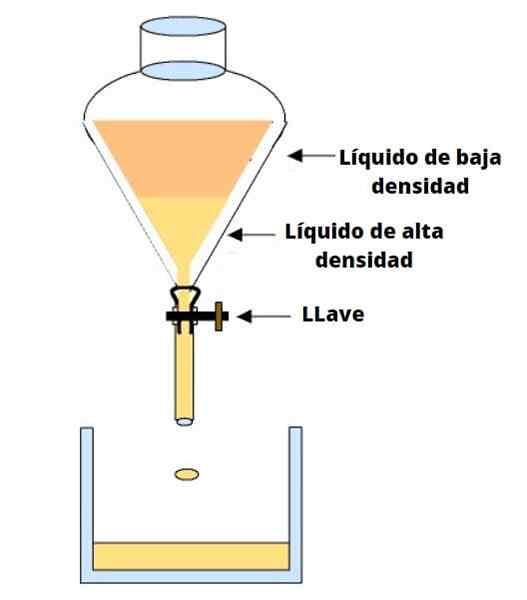 Décantation par le plaisir
Décantation par le plaisir Encore une fois, Gravity fait son travail, mais grâce à l'utilisation d'un entonnoir de décantation, qui permet à l'un des liquides de décider ou de jeter ci-dessous.
- Sublimation
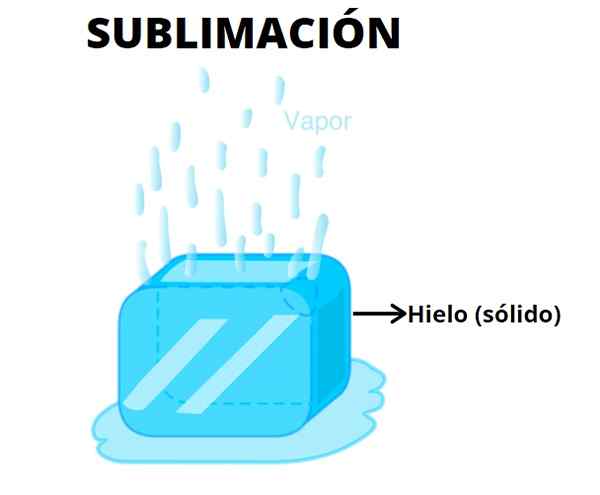 En sublimation, il y a un changement de l'état du solide au liquide
En sublimation, il y a un changement de l'état du solide au liquide La sublimation est une méthode de séparation spéciale utilisée pour séparer deux solides d'un mélange hétérogène. En principe, il a besoin d'au moins un des solides pour avoir une pression de vapeur très élevée, de sorte que lorsqu'elle est chauffée et l'application vide, elle s'évapore ou sublime en quittant le mélange derrière.
L'exemple classique de sublimation est la séparation d'un mélange d'iode-sable. L'iode, pour être un solide volatil, sublime comme des vapeurs violettes qui quittent le sable. Cependant, la sublimation peut également être appliquée pour séparer un mélange de héros sec, car la glace sèche (dioxyde de carbone solide) est beaucoup plus volatile que la glace normale (eau cristallisée).
 Un morceau de glace sec tombant dans un récipient à eau.
Un morceau de glace sec tombant dans un récipient à eau. De même, la sublimation peut être utilisée pour purifier les échantillons avec des solides parfumés, comme le camphre et autres.
- Évaporation
L'évaporation est peut-être l'une des méthodes de séparation plus lentes qui existent. En principe, en principe, le solvant du soluté est utilisé pour se séparer, ce qui termine l'apparence homogène d'une solution.
Peut vous servir: Aliquot (chimie)L'exemple classique est l'évaporation de l'eau de sucre pour obtenir des cristaux de sucre. Pour accélérer le processus, la chaleur d'une flamme est faite qui chauffe la solution jusqu'à ce que l'eau ou le solvant bouille.
 L'évaporation de l'eau dans la production de sel
L'évaporation de l'eau dans la production de sel L'évaporation est également utilisée pour obtenir des sels d'eau de mer ou pour sécher des gelée. De plus, l'évaporation lente et prolongée est l'une des étapes qui permet une excellente cristallisation.
- Distillation simple
 Équipement de distillation
Équipement de distillation Contrairement à la décantation, qui ne permet que la séparation des mélanges liquides-liquides, la distillation permet la séparation des mélanges liquides homogènes qui sont formés par un ou plusieurs composants liquides. Il est basé sur la différence dans les points d'ébullition des composants du mélange.
Par exemple, l'eau bouille autour de 100 ºC, tandis que l'acétone à 56 ºC. Ensuite, le mélange d'eau-acétone peut être distillé pour obtenir un extrait d'acétone.
De la même manière, cela se produit avec le mélange éthanol-eau, pour obtenir des solutions d'éthanol plus concentrées.
- Distillation fractionnée
 Équipement de distillation fractée
Équipement de distillation fractée La distillation fractionnaire est une distillation plus raffinée, dans le sens où elle permet de séparer les composants dont les points d'ébullition ne sont pas très différents. Comme il y a généralement plusieurs composants, chaque extrait est appelé fraction. Ainsi, plusieurs fractions à différentes propriétés sont obtenues.
La distillation fractionnaire de l'huile d'huile est le meilleur exemple de l'utilisation de cette méthode. De l'huile, plusieurs fractions se produisent, dont des produits tels que le gaz naturel, l'essence, le kéroseeno, l'acétone, le diesel, entre autres sont obtenus à leur tour.
- Chromatographie
 Séparation du colorant alimentaire par la comatographie en couche fine
Séparation du colorant alimentaire par la comatographie en couche fine La chromatographie est une méthode de séparation qui sauve également une certaine similitude avec la filtration. Il est beaucoup plus raffiné, sélectif et moins excessif en ce qui concerne le volume du mélange soumis à la séparation. Ce mélange peut être liquide (chromatographie liquide) ou gaz (chromatographie en phase gazeuse).
Au lieu d'utiliser un filtre, la chromatographie a besoin de ce qui est connu par phase stationnaire. Dans la chromatographie sur papier, en utilisant des marqueurs, le papier agit comme la phase stationnaire, c'est pourquoi le mélange se déplace lorsque les composants sont séparés (colorants).
 Scientifique en plaçant un tube à essai avec chromatographie en phase gazeuse
Scientifique en plaçant un tube à essai avec chromatographie en phase gazeuse La phase stationnaire par excellence est une colonne avec une garniture qui conserve les composants en fonction de ses interactions ou affinités. Ainsi, la chromatographie peut séparer les ions de différentes charges, molécules de différentes polarités ou tailles, etc.
Peut vous servir: Processus chimique: principes, types, exemplesLa chromatographie est essentielle pour analyser des mélanges complexes, évaluer l'action du médicament, détecter des composés chimiques spécifiques, entre autres exemples de son utilisation.
- Centrifugation
 Centrifugateur actif
Centrifugateur actif La centrifugation devient une "sédimentation forcée". En effet, grâce à l'accélération centripète, les particules solides en suspension sont liées à définir une phase. De cette façon, vous pouvez ensuite supprimer le surnageant ou prendre une aliquote pour effectuer une analyse.
La centrifugation est largement utilisée dans la séparation du plasma des cellules sanguines. Il sert également à séparer la graisse butyrique du lait, ou à accélérer la sédimentation de certains précipités.
Avec la chromatographie, la centrifugation est l'une des méthodes de séparation les plus sophistiquées des mélanges.
- Séparation magnétique
 Illustration de séparation magnétique
Illustration de séparation magnétique Comme son nom l'indique, il utilise le phénomène du magnétisme pour réaliser la séparation des composants de différents types de mélanges hétérogènes.
Un exemple serait un mélange de films de fer et de calcaire pulvérisé. Manuellement, nous pourrions procéder à séparer les petites pièces, mais cela prendrait beaucoup de temps et de patience. Au lieu de cela, un aimant puissant est utilisé qui attire des fichiers en fer et laisse la poussière de calcaire derrière.
Des mélanges similaires sont ceux de la sucre de fer, du sable de fer ou du coffre de fer. D'autres métaux tels que le nickel, le cobalt, l'affichage et le gadolinio, sont également attirés par les aimants.
Un autre exemple de séparation magnétique se produit dans certains décharges, où la ferraille est traitée et les aimants séparent des objets métalliques; comme les noix, les bâtons de golf, les clés, etc.
De toutes les méthodes de séparation, c'est peut-être le moins utilisé au sein du laboratoire ou de la vie quotidienne. Il est plus restreint que tout aux processus industriels.
Thèmes d'intérêt
Méthodes de séparation des mélanges homogènes.
Méthodes de séparation des mélanges hétérogènes.
Mélanges: composants et types.
Mélanges homogènes.
Mélanges hétérogènes.
Les références
- Whitten, Davis, Peck & Stanley. (2008). Chimie. (8e Ed.). Cengage Learning.
- Wikipédia. (2020). Processus de séparation. Récupéré de: dans.Wikipédia.org
- Amrit.Olabs.Édu.dans. (2012). Séparation des mélanges en utilisant différentes techniques. Récupéré de: Amrit.Olabs.Édu.dans
- Byju's. (s.F.). Méthodes de séparation. Récupéré de: byjus.com
- Université du Minnesota. (2020). Séparation du sable, du fer et du sel. Récupéré de: Chem.Umn.Édu
- María Estela Raffino. (9 mars 2020). Méthodes de séparation du mélange. Concept.de. Récupéré de: concept.de
- Chelsea Schuyler. (2020). Chromatographie, distillion et filtrer: méthodes de séparation des mélanges. Étude. Récupéré de: étudier.com
- « Caractéristiques de revue littéraire, parties, fonction, exemples
- Sources d'obligations commerciales, modalités, exemples »

