Concentration de molarité, unités, calcul, exercices
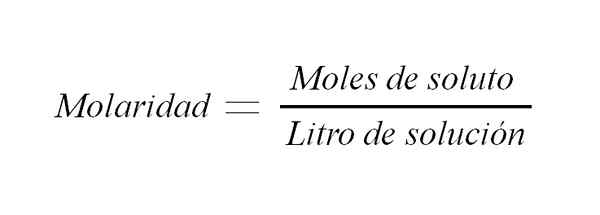
- 2366
- 394
- Lucas Schneider
La Molarité C'est la concentration d'une solution exprimée en taupes du soluté par litre de solution. Il est abrégé en M et exprime une relation entre la masse du soluté et le volume de la solution (m / v); Bien que d'une manière traditionnelle, cette relation est exprimée en poids de volume.
Une mol est le nombre d'atomes ou de molécules contenues dans le poids atomique ou moléculaire; Il est exprimé en grammes / mol. Une taupe équivaut à 6,02 · 1023 atomes ou molécules, connues sous le nom de numéro Avogadro.
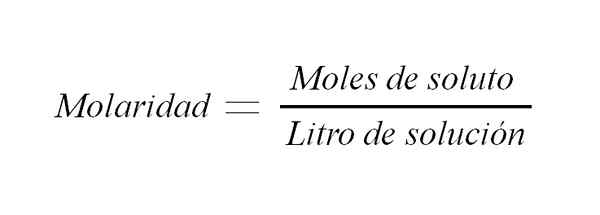 Formule de molarité. Source: Gabriel Bolívar.
Formule de molarité. Source: Gabriel Bolívar. Il existe d'autres moyens d'exprimer la relation entre la masse d'un soluté et le volume, notamment: le pourcentage de relation entre la masse du soluté et le volume de la solution, et la normalité. Ce dernier est exprimé comme le nombre d'équivalents d'un soluté par litre de solution.
Pendant ce temps, la moléalité, qui est définie comme le nombre de moles par kilogrammes de solvant, généralement en eau, exprime une relation entre la masse du soluté et la masse du solvant (m / m).
La forme d'expression de la concentration d'une solution en parties par million (PPM), exprime une relation entre une partie du soluté et un million de parties de la solution, généralement utilisée pour exprimer un rapport massial de masse (m / m). Mais vous pouvez exprimer un rapport masse-volume (m / v).
La concentration molaire, en plus de s'exprimer en moles par litre, peut être exprimée en millimoles / litre (solution millimolaire); micromoles / litre (solution micromolaire); etc.
Les problèmes de molarité peuvent être résolus en utilisant une méthode analytique et grâce à l'utilisation de "la règle de trois". Le choix d'une méthode dépendra de la possibilité d'utiliser l'une des méthodes.
[TOC]
Concentration molaire
Est utilisé pour exprimer la concentration d'un soluté dans une certaine solution de solution.
M = n / v (1)
Où m est égal à la molarité, n est le nombre de moles, et v le volume de la solution. Ainsi, la molarité d'une solution est le nombre de moles de soluté par volume de solution exprimée en litres.
D'un autre côté, le nombre de moles est
n = m / pm (2)
Étant la masse du soluté dissous et PM sa masse molaire.
Peut vous servir: aldéhydosRemplacement (2) dans (1):
M = (m / pm) / v
Unités
L'unité du système international pour la concentration molaire est mol / m3. Cela correspond à une solution millimolaire, car un m3 équivalent à 1.000 litres. Dans les branches de la chimie et de la biologie, la concentration molaire est généralement exprimée en moles / L. Cette unité est exprimée par le m (capital).
Une solution d'une mol / L, équivaut à un m; Une solution 10-3 moles / L, équivalent à 1 mm (millimolaire); et une solution 10-6 moles / L, équivalent à 1 µm (micromolaire).
Comment calculer la molarité?
Il est pratique d'utiliser les expressions indiquées ci-dessus, car cela garantit que le résultat de l'application de la formule donnera en taupes / litres, qui est la définition de la concentration molaire.
Ainsi, pour calculer la molarité d'une solution, il est nécessaire d'exprimer la concentration du soluté en g / l. Puis découvrez le poids moléculaire du soluté (g / mol) et trouvez le quotient entre la concentration et le poids moléculaire. Le résultat obtenu est la molarité exprimée en moles / litre.
Passer de la molarité à la moléalité
Un fait nécessaire pour passer de la molarité à la moléalité est de connaître la densité de la solution. Cela permet de connaître la masse de la solution, une exigence essentielle pour le calcul de la moléalité.
Premier pas
Vous devez d'abord passer de la concentration molaire aux grammes / litres. Pour ce faire, il suffit de multiplier la molarité de la solution par le poids moléculaire du soluté.
Grammes / litre du soluté = molarité (moles / litre) · Poids moléculaire du soluté (grammes / mol).
Cela permet d'obtenir la masse du soluté en 1 L de solution.
Deuxième pas
Alors il est nécessaire de calculer la masse de la solution. Pour ce faire, la densité de la même chose est utilisée. Habituellement, la densité est exprimée en grammes / centimètres cubes ou en millilitre.
Masse de solution (g) = volume de solution (ml) · densité (g / ml)
Troisième étape
Obtenir la masse de solvant. Comme la masse de la solution est égale à la masse du soluté plus la masse du solvant, pour obtenir la masse du dernier est suffisante pour soustraire de la masse de la solution (étape 2) la masse du soluté (étape 1).
Il peut vous servir: oxyde perchlorique (CL2O7)Quatrième étape
Enfin, vous devez passer la masse du soluté (g) de la solution à la masse de soluté qui correspond à 1.000 g ou 1 kg de solvant. Pour ce faire, il suffirait de faire une règle de trois opérations mathématiques simples ou autres.
Cinquième étape
Divisez g de soluté / 1000 g de solvant entre le poids moléculaire du soluté (g / mol) pour obtenir la moralité de la solution.
Exemple numérique
Une solution de glucose de 3 m (180 g / poids moléculaire molaire) a une densité de 1,15 g / ml. Calculez la moléalité de cette solution.
Nous calculons d'abord les grammes de glucose dissous dans un litre de solution:
g / l = 3 moles / l · 180 g / mol
= 540 g / L
Ensuite, nous calculons la masse de la solution à partir de sa densité:
g de la solution (masse) = 1.000 ml · 1,15 g / ml
= 1.150 g
La masse de solvant est donnée par la différence:
Masse de solvant = masse de solution - masse de soluté
= 1.150 g - 540 g
= 610 g
Mais 610 g ne sont pas 1000 g de solvant comme stipulant la définition de la molélité. Par conséquent, combien de grammes de glucose doivent être calculés sont dissous dans 1000 g de solvant:
Masse de soluté = 540 g de soluté · (1.000 g de solvant / 610 g de solvant)
= 885,25 g
Et enfin, la molélité est calculée en renvoyant les grammes en taupes:
Molality = (885,25 g de soluté / 180 g / mol)
= 4,92 mols soluté / kg de solvant
= 4,92 m
Problèmes résolus
Problème 1
Combien de sulfate de cuprique sera nécessaire pour préparer 500 ml d'une solution de 0,4 m? Exprimer le résultat en grammes. Poids moléculaire du sulfate de cuprique (Cuso4): 160 g / mol.
Nous déterminons d'abord les moles qui doivent être dissoutes dans une telle solution:
M = n / v
n = m · v
n = (0,4 moles / L) · 0,5 L
= 0,2 moles
Sachant alors que le nombre de moles de sulfate cuprique peut être obtenu sa masse
N = m / pm
m = n · poids moléculaire
M = 0,2 moles · 160 g / mol
= 32 g de cuso4
C'est-à-dire que 32 grammes de ce sel doivent être dissous dans 500 ml de solvant.
Problème 2
Quel volume d'une solution est nécessaire pour dissoudre 0,4 moles de soluté, il a une concentration de 0,25 m?
Le volume de la solution est obtenu à partir du concept de molarité
Peut vous servir: Samario: caractéristiques, structure, obtention, utilisationsM = n / v
V = n / m
V = 0,4 moles / (0,25 moles / L)
= 1,6 L
Cela signifie que la solution doit avoir un volume de 1,6 litre pour obtenir une telle concentration de 0,25 m.
Problème 3
Une masse de 8 g d'hydroxyde de sodium (NaOH) est dissoute dans 60 g d'une solution qui a une densité de 1,6 g / ml. Quelle sera la molarité de la solution? Poids moléculaire de l'hydroxyde de sodium: 40 g / mol.
Les moles de beauté de Naoh doivent être calculées en premier:
N = m / pm
= 8 g d'hydroxyde de sodium / (40 g / mol)
= 0,2 moles
Maintenant, le volume de la solution est calculé:
M = V · D
V = 60 g /(1,6 g / ml)
V = 37,5 ml
Pour obtenir la molarité, le volume de la solution en litres doit être placé:
V = 37,5 ml · 10-3 L / ml
= 0,0375 L
M = 0,2 moles / 0,0375 L
5,33 moles / L
5,33 m
Problème 4
Calculez la molarité d'une solution d'acide chlorhydrique (HCl) avec une densité de 1,25 g / ml et une concentration de 35%, une masse exprimée / masse. Poids moléculaire de l'acide chlorhydrique: 36,5 g / mol.
La masse de 35% d'acide chlorhydrique est déterminée
M = V · D
M = 1.000 ml · 1,25 g / ml
= 1.250 g
Mais tout n'est pas du HCL, mais il y a aussi de l'eau:
Masse HCl = 1.250 g · (35/100)
= 437,5 g
Ce qui est la même chose que de dire que dans un litre de solution HCl à 35%, il y a 437,5 grammes de HCL.
Ensuite, les moles de HCL sont calculées, pour déterminer ensuite la molarité:
N = m / pm
n = (437,5 g / l) / (36,5 g / mol)
= 11,98 moles / L
Molarité = 11,98 m
Problème 5
Calculez la molarité d'une solution contenant 5 g de NaCl dans 2 L de solution. Poids moléculaire du chlorure de sodium: 58,5 g / mol.
Les moles / L de NaCl peuvent être obtenues en une seule étape:
Molarité = (solution NaCl / 2 L 5 g) x (1 mol NaCl / 58,5 g de NaCl)
= 0,043 moles / L
Molarité = 0,043 m
Une autre procédure pourrait être:
G / L de NaCl = 5 g / 2 L
= 2,5 g / L
Mules / L = (2,5 g / L) / (58,5 g / mol)
= 0,043 moles / L
= 0,043 m
Les références
- Rodríguez, M. (2007). Chimie. Scomniana Editorial Foundation
- Whitten, Davis, Peck & Stanley. (2008). Chimie. (8e Ed.). Cengage Learning.
- Wikipédia. (2019). Molarité. Récupéré de: est.Wikipédia.org
- Atarés Huerta. (s.F.). Molarité et moléalité. [PDF]. Récupéré de: Riunet.UPV.est
- Softchols. (2019). Formule de molarité. Récupéré de: softschools.com
- « Caractéristiques spéciales des composés, formation, utilisations
- Difficultés de consolidation d'un projet Nation »

