Structure du métabisulfite de sodium (NA2S2O5), propriétés, utilisations, risques

- 3723
- 165
- Paul Dumas
Il le métabisulfite de sodium C'est un composé inorganique formé de deux ions de na du sodium+ et un métabisulfite ou un ion disulfite2SOIT52-. Sa formule chimique est na2S2SOIT5. C'est un solide blanc cristallin. Il est utilisé comme agent antioxydant et antimicrobien dans une variété de produits pharmaceutiques et fonctionne comme conservateur dans de nombreuses préparations alimentaires.
Puis un2S2SOIT5 Il sert à traiter la farine pour fabriquer des biscuits et des bonbons à pâtisse.
 Métabisulfite de sodium na2S2SOIT5 solide. Aucun auteur lisible par machine fourni. Walkerma a supposé (sur la base des réclamations du droit d'auteur). [Domaine public]. Source: Wikimedia Commons.
Métabisulfite de sodium na2S2SOIT5 solide. Aucun auteur lisible par machine fourni. Walkerma a supposé (sur la base des réclamations du droit d'auteur). [Domaine public]. Source: Wikimedia Commons. Il est utilisé dans de nombreux aliments transformés pour les empêcher d'être attaqués par des champignons et des bactéries. Parmi ces aliments se trouvent des fromages, des jus de fruits, des sauces, des margarines, etc.
Cependant, comme certains effets négatifs sur la santé des gens ont été remarqués, les organismes autorisés contrôlent la quantité maximale de métabisulfite de sodium2S2SOIT5 qu'ils doivent contenir ces aliments.
Les autres applications NA2S2SOIT5 Ils sont généralement basés sur leurs propriétés réductrices (l'opposé de l'oxydation), par exemple pour réduire la quantité de chlore dans les eaux traitées, comme le blanchissement de la laine, dans les formules cosmétiques, entre autres utilisations.
[TOC]
Structure
Le métabisulfite de sodium est formé par deux ions de sodium+ et un ion bisulfite s2SOIT52-. Ce dernier a deux atomes de soufre unis ensemble et cinq atomes d'oxygène répartis entre ces.
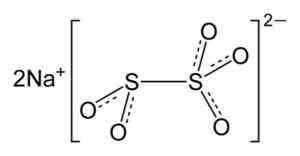 Structure chimique du métabisulfite de sodium2S2SOIT5. Auteur: Benjah-bmm27. Source: Wikimedia Commons.
Structure chimique du métabisulfite de sodium2S2SOIT5. Auteur: Benjah-bmm27. Source: Wikimedia Commons. Nomenclature
-Le métabisulfite de sodium
-Pyrosulfite de sodium
-Disulfite de sodium
-Dysodium disulfite
Propriétés
État physique
Incolore, blanc ou jaunissant cristallin. Cristaux hexagonaux.
Poids moléculaire
190,11 g / mol
Point de fusion
À des températures supérieures à 150 ° C est décomposée.
Poids spécifique
1,4 à 25 ° C / 4 ° C
Solubilité
Très soluble dans l'eau: 66,7 g / 100 g d'eau.
Peut vous servir: oxygène moléculaire: structure, propriétés, utilisationspH
Ses solutions aqueuses sont acides. Une solution de 10% a un pH de 4,0-5,5.
Propriétés chimiques
Lors de la dissolution dans l'eau, c'est un acide corrosif. Il a des propriétés réducteurs et antioxydantes.
S'il est exposé à l'air, oxyde lentement le sulfate de sodium2Swin4, perdre également une partie de son contenu2.
Réagit avec l'eau pour donner du bisulfite de sodium3, dioxyde de soufre2 et sulfite de sodium na2Swin3.
Il a une légère odeur de soufre. Ce n'est pas du carburant, mais sous la chaleur peut générer des gaz toxiques.
Obtention
Le métabisulfite de sodium peut être obtenu en passant un excès de dioxyde de soufre à gaz2 Pour une solution de carbonate de sodium NA2CO3.
Utilisations dans la nourriture
Comme conservateur
Puis un2S2SOIT5 C'est un antioxydant. Il sert de conservateur et d'inhibiteur de certains micro-organismes. Son effet antimicrobien est optimal en dessous de pH = 4, comme dans les jus de fruits.
Il permet de prévenir la détérioration et de se noircir de certains aliments plus lentement. Il a été utilisé par exemple pour éviter l'assombrissement des patates douces.
Il est utilisé pendant la récolte de crevettes marines pour empêcher la formation de taches noires. Les crevettes sont immergées dans une solution de métabisulfite sur la glace.
 Parfois, les crevettes sont immergées dans une solution aqueuse de métabisulfite de sodium pour les empêcher de se détériorer. Auteur: Aakashkhatu1998. Source: Pixabay.
Parfois, les crevettes sont immergées dans une solution aqueuse de métabisulfite de sodium pour les empêcher de se détériorer. Auteur: Aakashkhatu1998. Source: Pixabay. Il s'agit d'un antioxydant efficace et améliore la rétention d'acide ascorbique (vitamine C) dans les fruits et jus séchés. Dans celles-ci, certains types de bactéries, de champignons et de levure.
Il a été utilisé en Afrique du Sud pour contrôler la détérioration et inhiber l'assombrissement des fruits de lichi. Cependant, il semble que le goût dudit fruit change légèrement.
Les autres aliments utilisés sont le fromage, diverses boissons, la margarine, les sauces, les bonbons et le poisson.
Dans l'industrie du vin et d'autres boissons
Dans les raisins après la récolte, il est utilisé comme fongicide, car certains champignons peuvent pousser sur ce fruit. Ensuite, agissez sur certains micro-organismes spécifiques, ce qui le rend utile dans l'industrie du vin car il permet de contrôler sa fermentation.
Peut vous servir: 10 exemples de liens covalents non polairesLe métabisulfite résiduel est efficace après la fermentation du vin pour éviter la croissance des levures tolérantes à l'alcool.
Il a également été utilisé dans le jus de pomme et le cidre pour contrôler certains micro-organismes pathogènes tels que Escherichia coli.
Pour traiter certaines farines, céréales et amidons
Il sert à conditionner la masse de certains aliments au four. Il agit comme un agent réducteur dans la fabrication de biscuits, en particulier les décontractés en matières grasses et faibles en sucre, et dans les bonbons pâtissiers.
Le métabisulfite réagit avec les liaisons S-S des protéines contenues dans la farine de pâte avec laquelle les biscuits et les bonbons sont préparés, l'adoucissant, le rendant plus extensible et moins élastique.
L'un des objectifs est d'empêcher que la pâte soit respirée, avant ou pendant la cuisson. Cependant, son utilisation dans la masse des cookies n'est pas toujours acceptée et d'autres alternatives sont préférées.
 Certains fromages, confitures et biscuits peuvent contenir du métabisulfite de sodium comme conservateur. Auteur: Steve Buisinne. Source: Pixabay.
Certains fromages, confitures et biscuits peuvent contenir du métabisulfite de sodium comme conservateur. Auteur: Steve Buisinne. Source: Pixabay. Il sert également à blanchir les amidons comestibles et à adoucir les grains de maïs pendant le processus de broyage humide.
Aliments dans lesquels il ne doit pas être utilisé
La Food and Medicine Administration des États-Unis, ou FDA (pour son acronyme pour l'anglais Food and Drug Administration) Métabisulfite de sodium marqué2S2SOIT5 En tant que substance "considérée comme généralement sûre".
Cependant, il a été reconnu par cet corps comme un composé antitiamine ou anti-amitamine B1.
Par conséquent, il ne doit pas être utilisé dans les viandes, ni dans les aliments source de vitamine B1. Il ne doit pas non plus être utilisé dans des fruits ou des légumes vendus crus aux consommateurs ou qui sont présentés comme frais.
Peut vous servir: chlorite de sodium (Naclo2): structure, propriétés, utilisations, risquesSelon certaines sources consultées si elles sont utilisées dans des concentrations supérieures à 10 mg / kg de nourriture, elle doit être signalée sur l'étiquette de ce.
Autres utilisations
Autres applications NA2S2SOIT5 dessous.
-En tant qu'agent réducteur dans les formules cosmétiques et comme antioxydant par exemple dans les produits de soins capillaires.
-Comme antioxydant dans les préparations pharmaceutiques, comme les sirops ou les fluides injectables. Il est utilisé dans les préparations acides. Il a une certaine activité antimicrobienne, en particulier le pH acide.
-En tant que réactif de laboratoire, par exemple pour préserver l'histamine lorsque son analyse est effectuée.
 Certains médicaments liquides peuvent contenir NA2S2SOIT5 Comme conservateur. Auteur: Steve Buisinne. Source: Pixabay.
Certains médicaments liquides peuvent contenir NA2S2SOIT5 Comme conservateur. Auteur: Steve Buisinne. Source: Pixabay. -En tant qu'agent réducteur dans le développement de photographies.
-Pour réduire le chlore dans les processus industriels, le traitement de l'eau et des eaux usées.
-Dans l'industrie textile: comme blanchie en laine, en tant qu'agent anticloro après le blanchiment d'argent, pour réduire certains colorants et solubiliser d'autres.
-Pour produire du dioxyde de soufre2 Sur le site d'utilisation. Par exemple dans les silos d'herbe frais, le so2 Produit par le métabisulfite de sodium développe rapidement l'acidité et permet la conservation du matériau, car la fermentation prendrait trop de temps.
 La laine peut être blanchie avec du métabisulfite de sodium. Auteur: Jaclou DL. Source: Pixabay.
La laine peut être blanchie avec du métabisulfite de sodium. Auteur: Jaclou DL. Source: Pixabay. Des risques
-Si le na est inhalé2S2SOIT5 solide est toxique. Le contact direct irrite fortement la peau, les muqueuses et les tissus. Ce sont des yeux irritants et un système respiratoire.
-Si vous êtes ingéré directement, vous pouvez produire des douleurs abdominales, une diarrhée, des nausées et des vomissements.
-C'est corrosif.
-On dit que certains asthmatiques sont dangereusement sensibles aux petites quantités de métabisulfite dans les repas.
-C'est nocif pour les organismes aquatiques.
Les références
- Cauvain, s.P. (2017). MATIÈRES PREMIÈRES. Dans les problèmes de cuisson résolus (deuxième édition). Récupéré de ScienceDirect.com.
- OU.S. Bibliothèque nationale de médecine. (2019). Métabisulfite sodium. Centre national d'information sur la biotechnologie. Récupéré de pubchem.NCBI.NLM.NIH.Gouvernement.
- Sivakumar, D. et Korsten, L. (2011). Litchi (Lush Chinensis Sonn.). Dans la biologie et la technologie les plus compensées des fruits tropicaux et subtropicaux: cocona à la mangue. Récupéré de ScienceDirect.com.
- Danyluk, M.D. et al. (2012). Décontamination microbienne des jus. En décontamination microbienne dans l'industrie alimentaire. Récupéré de ScienceDirect.com.
- Wieer, H. (2012). L'utilisation d'agents redox dans la fabrication de brutad. En mélange (deuxième édition). Récupéré de ScienceDirect.com.
- Ercan, s. et al. (2015). Induction de la voie inflammatoire de l'oméga 6 par le métabisulfite de sodium dans le foie du rat et son atténuation par la ghréline. Lipides de la santé et des maladies (2015) 14: 7. NCBI a récupéré.NLM.NIH.Gouvernement.
- « Formules de chaleur et unités, caractéristiques, comment est mesuré, exemples
- Solution chauffage comment calculé, applications et exercices »

