Fondation d'immunofluorescence, protocole et applications
- 2288
- 337
- Raphaël Meyer
La immunofluorescence Il s'agit d'une puissante technique d'immunomarcy qui utilise des anticorps unis de manière covalente aux molécules fluorescentes pour identifier des cibles spécifiques dans des échantillons de cellules fixés sur un support solide.
Cette technique observation microscopique avec spécificité immunitaire, ce qui permet d'observer l'observation des cellules vivantes ou mortes qui peuvent avoir de minuscules quantités d'antigènes. Il est largement utilisé à la fois dans le domaine de la recherche et dans le diagnostic clinique de diverses pathologies.
 Immunomarité des filaments d'actine dans les cellules cardiomyocytaires (Source: PS1415 [CC BY-SA 4.0 (https: // CreativeCommons.Org / licences / by-sa / 4.0)] via Wikimedia Commons)
Immunomarité des filaments d'actine dans les cellules cardiomyocytaires (Source: PS1415 [CC BY-SA 4.0 (https: // CreativeCommons.Org / licences / by-sa / 4.0)] via Wikimedia Commons) Cette technique principalement qualitative (avec certaines variantes quantitatives) doit faire spécifiquement avec la visualisation d'un échantillon par le produit d'un fluorophore, qui est une molécule fluorescente attachée à un anticorps et qui est capable de s'exciter à une certaine longueur d'onde.
Dans le contexte cellulaire, il est très utile d'étudier la présence / absence et l'emplacement subcellulaire des protéines. La technique a été utilisée dans ses débuts dans le domaine clinique pour le diagnostic de virus tels que la grippe et par la suite pour de nombreuses autres maladies infectieuses.
C'est une technique d'une grande sensibilité, et avec la bonne équipe de microscopie, il peut avoir une très bonne résolution. Il faut, pour son observation, l'utilisation de microscopes confocaux ou épifluorescence.
Cependant, bien qu'il soit très populaire, vous pouvez présenter des problèmes importants concernant l'obtention d'une fluorescence non spécifique qui génère un certain "bruit" en arrière-plan, ce qui limite souvent la lecture appropriée des résultats.
[TOC]
Base
L'immunofluorescence est basée sur l'exploitation du phénomène biologique de la réaction d'interaction entre un anticorps et un antigène. Il doit faire spécifiquement avec la visualisation ou la détection de cette réaction lorsqu'il est passionnant de molécules fluorescentes à une longueur d'onde spécifique.
Un anticorps est une protéine d'immunoglobuline sécrétée à partir de cellules B actives et est spécifiquement générée contre un antigène, qui peut être jointe à une grande affinité et spécificité. L'immunofluorescence utilise des immunoglobulines IgG, qui se trouvent solubles dans le sérum sanguin.
Les anticorps sont des molécules jusqu'à 950 kDa composées de deux peptides courts (légers) et deux longueurs sous la forme de "Y" (lourd). Les chaînes légères et lourdes sont divisées en deux domaines: une variable, capable de reconnaître l'antigène, et une autre constante ou conservée, caractéristique de chaque espèce.
Les antigènes sont fonctionnellement définis comme des molécules qui peuvent être reconnues par un anticorps et sont principalement des protéines. Lorsqu'un animal est exposé à un antigène, les lymphocytes du système immunitaire sont activés, produisant des anticorps spécifiques contre lui et fonctionnant comme un système de défense.
Un antigène, comme une protéine, par exemple, peut avoir plus d'un épitope ou un lieu de reconnaissance pour un anticorps, de sorte que le sérum de l'animal exposé à un antigène peut avoir des anticorps polyclonaux contre différentes régions de la même protéine.
Il peut vous servir: épiderme de l'oignonL'immunofluorescence exploite donc la capacité d'un animal à produire des anticorps polyclonaux contre un antigène spécifique afin de le purifier et de l'utiliser plus tard pour la détection du même antigène dans d'autres contextes.
Parmi les colorants ou molécules fluorescentes les plus utilisés pour certaines techniques d'immunofluorescence figurent la fluorescéine isochianate de la fluorescéine (FITC), de la tétraméthylrodamine-5 et 6 (Tritc), de nombreuses cyanines telles que Cy2, Cy3, Cy5 et Cy7 et colorants appelés Alexa Fluor®, comme l'Alexa, comme l'Alexa, Fluor®448.
Protocole
Le protocole d'immunofluorescence varie en fonction de nombreux facteurs, cependant, et en général, englobe une séquence linéaire d'étapes consistant en:
- Préparation des feuilles et des cellules
- Échantillon de fixation
- Perméabilisation
- Blocage
- Immunotive ou immunomarcaje
- Assemblage et observation
-préparation
Des échantillons
La préparation des échantillons dépendra de leur nature et du type d'expérience à effectuer. Ensuite, le cas le plus simple sera expliqué, ce qui implique l'utilisation de cellules en suspension.
Les cellules de suspension, c'est-à-dire dans un milieu de culture liquide, doivent d'abord être séparées de cela par centrifugation et doivent ensuite être lavées avec une solution tampon ou "amortir" isosmotique, qui préserve son intégrité.
Normalement, un tampon phosphate-saline est utilisé connu sous le nom de PBS, dans lequel les cellules sont remis en suspension.
Des draps
Les feuilles utilisées pour l'observation microscopique, où les cellules seront réglées pour les traitements en aval correspondants, doivent également être soigneusement préparés.
Ceux-ci sont couverts ou «sensibilisés» avec une solution polysine, un polymère synthétique qui servira de «colle moléculaire» entre les cellules et le soutien solide, grâce à l'interaction électrostatique entre les charges positives de leurs groupes amino et les charges négatives de protéines qui couvrent cellules.
Échantillon de fixation
Ce processus consiste à immobiliser les protéines qui sont à l'intérieur cellulaire afin de garder leur emplacement spatial intact. Les molécules utilisées devraient pouvoir traverser tous les types de membranes cellulaires et former des cadres avec des protéines covalentes.
Le formaldéhyde et le paraformaldéhyde, le glutaraldéhyde et même le méthanol sont largement utilisés, avec lesquels des échantillons de cellules sont incubés pendant un certain temps, puis les lavant avec une solution tampon isosmotique.
Après la fixation des cellules, il continue de les rejoindre sur les feuilles précédemment sensibilisées avec de la polysine.
Perméabilisation
Selon le type de test effectué, il sera nécessaire de perméabiliser ou non les cellules à l'étude. Si ce qui est recherché, c'est connaître l'emplacement, la présence ou l'absence, d'une certaine protéine à la surface cellulaire, la perméabilisation ne sera pas nécessaire.
Peut vous servir: phosphatidylinositol: structure, formation, fonctionsD'un autre côté, si vous voulez connaître l'emplacement d'une protéine à l'intérieur de l'intérieur cellulaire, la perméabilisation est indispensable et consistera à incuber des échantillons avec Triton X-100, un détergent capable de perméabiliser les membranes cellulaires.
Blocage
Une étape fondamentale dans toutes les techniques immunologiques bloque. À ce stade de la procédure, le blocus consiste à couvrir, dans les feuilles sensibilisées, tous les sites avec des molécules de polyesine auxquelles les cellules n'étaient pas adhérées. C'est-à-dire qu'il empêche toute union non spécifique.
Normalement pour le blocage des solutions avec l'albumine de lactosérum Bovine (BSA) est utilisé dans le tampon PBS et les meilleurs résultats sont obtenus, plus il est le temps d'incubation avec cette solution. Après chaque étape, y compris le blocus, il est nécessaire de retirer la solution restante en lavant.
Immunotive ou immunomarcaje
La procédure d'immunomarité ou d'immunomarité dépendra principalement s'il s'agit d'une immunofluorescence directe ou indirecte (voir plus loin).
S'il s'agit d'une immunofluorescence primaire ou directe, les échantillons seront incubés avec les anticorps souhaités, qui doivent être couplés aux colorants fluorescents. La procédure d'incubation consiste à faire une dilution de l'anticorps dans une solution que BSA contiendra également mais dans une proportion inférieure.
Lorsque le cas est celui d'une immunofluorescence secondaire ou indirecte, deux incubations consécutives doivent être faites. D'abord avec les anticorps souhaités, puis avec les anticorps capables de détecter les régions constantes des immunoglobulines primaires. Ce sont ces anticorps secondaires qui sont unis de manière covalente aux fluorophores.
La technique est très polyvalente, permettant des marques simultanées de plus d'un antigène par échantillon, tant qu'elles ont des anticorps primaires couplés à différents fluorophores, dans le cas d'une immunofluorescence directe.
Pour les marques simultanées en immunofluorescence indirecte, il est nécessaire.
Comme le blocus, l'incubation avec des anticorps donne de meilleurs résultats, plus. Après chaque étape, il est nécessaire de laver les anticorps excédentaires qui n'ont pas rejoint les échantillons et dans l'immunofluorescence secondaire, il est nécessaire de bloquer avant d'ajouter l'anticorps secondaire.
Certaines techniques utilisent d'autres colorants qui n'ont rien à voir avec l'immunomarité, comme la coloration à l'ADN nucléaire avec Dapi Fluorophore.
Assemblage et observation
Pendant le temps d'incubation final avec des fluorophores, il est nécessaire que les échantillons restent dans l'obscurité. Pour l'observation du microscope, c'est courant.
Gars
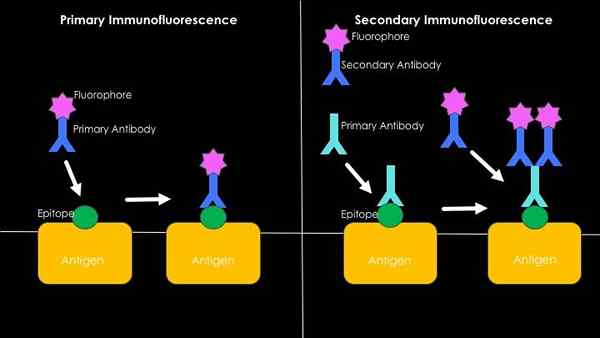 Résumé graphique de l'immunofluorescence directe et indirecte (Source: Westhayl618 [CC BY-SA 4.0 (https: // CreativeCommons.Org / licences / by-sa / 4.0)] via Wikimedia Commons)
Résumé graphique de l'immunofluorescence directe et indirecte (Source: Westhayl618 [CC BY-SA 4.0 (https: // CreativeCommons.Org / licences / by-sa / 4.0)] via Wikimedia Commons) Immunofluorescence directe ou primaire
Cela a à voir avec la détection des antigènes grâce à l'utilisation d'anticorps fluorescents. Le principal avantage de l'utilisation de cette technique est sa vitesse, cependant, de nombreux cas d'union non spécifique peuvent se produire dans le processus, en particulier lors de l'étude des sérums humains, car ils sont riches en anticorps très hétérogènes.
Peut vous servir: les 5 branches de la biotechnologie principaleImmunofluorescence indirecte ou secondaire
Il est également connu sous le nom de technique «sandwich» et cela implique le développement de la technique en deux étapes. Le premier a à voir avec l'utilisation d'un anticorps non fluorescent et de son union à l'antigène d'intérêt.
Contre la région constante de ce premier anticorps (qui servira désormais d'antigène) un deuxième anticorps capable de reconnaître qu'il est utilisé, qui est associé à une molécule fluorescente.
L'apparition d'un signal fluorescent sera le résultat de la reconnaissance spécifique entre le premier anticorps non fluorescent et l'antigène d'intérêt; La présence de cet premier anticorps conditionne celle de la seconde, qui est étiquetée et grâce à laquelle la présence ou l'absence de l'antigène peut être déterminée.
En dépit d'être une technique qui consomme beaucoup plus longtemps que l'immunofluorescence directe (car elle comprend une étape plus d'incubation), cette technique n'implique pas la conception d'un anticorps fluorescent pour chaque antigène étudié, ce qui résulte, en termes économiques, plus viable viable.
De plus, il s'agit d'une technique plus sensible en termes d'amplification du signal, car plus d'un anticorps secondaire peut rejoindre la région constante de l'anticorps primaire, amplifiant ainsi l'intensité du signal fluorescent.
Applications
Comme indiqué précédemment, l'immunofluorescence est une technique extrêmement polyvalente, à laquelle la multiplicité des utilisations dans les domaines scientifiques et cliniques a été donnée. Il peut être utilisé pour répondre aux questions écologiques, génétiques et physiologiques concernant de nombreux organismes.
Parmi les applications cliniques, il est utilisé pour le diagnostic direct de certaines maladies dermatologiques, que ce soit en utilisant une immunofluorescence directe ou indirecte sur le tissu épithélial des patients étudiés.
Des techniques d'immunofluorescence ont été organisées dans des organismes unicellulaires tels que les levures pour visualiser les microtubules intranucléaires et cytoplasmiques, l'actine et les protéines associées, les filaments 10 nm et autres constituants du cytoplasme, des murs membranaires et cellulaires.
Les références
- ABCAM, Immunocytochimie et protocole d'immunofluorescence. Récupéré d'Abcam.com
- Greph, C. (2012). Colorants fluorescents. Récupéré de Leica-microsystèmes.com
- Miller, D. M., & Shakest, D. C. (Année mille neuf cents quatre-vingts-quinze). Microscopie à immunofluorescence. Dans Méthodes en biologie cellulaire (Vol. 48, pp. 365-394). Academic Press, Inc.
- Odell, je. D., & Cook, D. (2013). Techniques d'immunofluorescence. Journal of Investigative Dermatology, 133, 1-4.
- Prince, B. J. R., Adams, un. ET. M., Druain, D. g., & Brian, k. (1991). Méthodes d'immunofluorescence pour YEAS. Dans Méthodes d'enzymologie (Vol. 194, pp. 565-602). Academic Press, Inc.
- Schaeffer, m., Orsi, e. V, & widelock, D. (1964). Applications de l'immunofologie dans la virologie de la santé publique. Revues bactériologiques, 28(4), 402-408.
- Vrieling, e. g., & Anderson, D. M. (mille neuf cent quatre vingt seize). Immunofluorescence dans la recherche sur le phytoplancton: applications et potentiel. J: Phycol., 32, 1-16.
- « Areolar Speed Comment il est calculé et résolu les exercices
- Gouvernement Alberto Fujimori Premier et deuxième gouvernement »

