Indicateurs de pH

- 4667
- 807
- Prof Noah Collet
Quels sont les indicateurs de pH?
Les indicateurs de pH Ce sont des substances qui servent à déterminer la quantité de pH trouvée dans un milieu spécifique. Lorsque vous parlez du concept de pH, cela représente la concentration des ions hydronium (H3SOIT+) qui est présent dans une solution aqueuse.
De même, il est mesuré sur une échelle logarithmique négative entre 0 et 14, où des solutions à pH inférieures à 7 sont considérées. Ce paramètre est exprimé comme suit avec l'équation Henderson-Hasselbalch: Ph = PKA + Logdix ([POUR-]/[HA]).
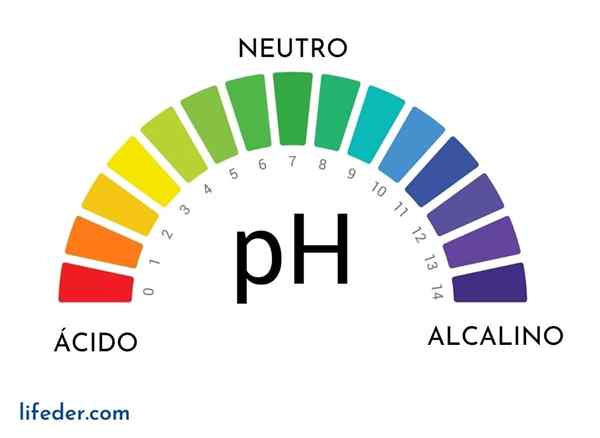
Dans l'expression précédente, la PKA représente le logarithme négatif de la constante de dissociation acide et les concentrations molaires [A-] et [ha] sont ceux de l'acide faible et sa base conjuguée, respectivement. Connaître le pH vous permet d'étudier la qualité de l'eau et de la nourriture et de pouvoir maintenir la répétabilité d'un produit chimique élaboré.
Types d'indicateurs
Il existe trois principaux types d'indicateurs de pH:
- Indicateurs liquides acides, qui fonctionnent selon une certaine plage de pH.
- Les papiers, les bandes et autres matériaux indicateurs qui changent de couleur tel qu'il est ajouté un échantillon ou un soda à sa surface.
- Ph-Mmetters numériques, qui mesurent la différence électrique potentielle entre deux électrodes.
Indicateurs liquides
 Indicateurs liquides
Indicateurs liquides Les indicateurs liquides sont des acides faibles ou des bases organiques qui ont des couleurs variantes en fonction de leur acide ou de leur forme de base. Ceux-ci fonctionnent dans des gammes limitées, la couleur variable une fois celle-ci, et cesse pour varier la couleur lorsque le niveau maximum de la plage est atteint.
Peut vous servir: dichlorométhane: structure, propriétés, utilisations, toxicitéPour fonctionner, ils ne doivent être utilisés que dans des solutions où un changement de couleur peut être observé (de préférence incolore).
Il existe un grand nombre d'indicateurs liquides de différentes couleurs et plages de pH, y compris le rouge de Cresol (jaune rouge dans une plage de 0,2 à 1,8), le rouge de méthyle (rouge à jaune dans une plage de 4, 2 à 6,2), Bromocresol Vert (rose au bleu / vert de 4,2 à 5,2) et phénolphtaleine (incolore au rose dans une plage de 8,0 à 10,0).
Ces indicateurs sont populaires pour les diplômes en chimie analytique, bien qu'un certain niveau de formation doit être nécessaire pour effectuer cette pratique de manière précise.
Indicateurs ou bandes papiers
 Scientifique utilisant une bande d'indicateur de pH
Scientifique utilisant une bande d'indicateur de pH Il existe plusieurs types de papiers utilisés pour mesurer le pH, mais le plus connu est le papier décisif si appelé, qui est fait avec une poudre qui provient de lichens.
Le papier ShortaSol sert à savoir si une solution liquide ou gazeuse est acide ou basique (sans savoir quel sera son pH exact ou une estimation), et se présente en deux présentations: bleu et rouge.
Le papier brillant bleu change en rouge dans des conditions acides et le papier de germe rouge change en bleu dans des conditions de base ou alcalin, pouvoir recycler pour effectuer le test de manière inverse une fois que le papier a déjà changé la couleur.
Les limites connues du papier comme son incapacité à offrir une valeur exacte ou estimée du pH et la capacité de passer à d'autres couleurs lorsqu'il réagit avec certains composés, ce qui l'a fait remplacer par le liquide et / ou le ph-métros indicateurs.
pH -metros
 pH-pH numérique
pH-pH numérique Les méthodes pH sont nées de la nécessité d'analystes de laboratoire pour obtenir des valeurs exactes de ce paramètre, ce qui n'était pas possible avec des indicateurs de papier ou des indicateurs liquides.
Peut vous servir: cation: formation, différences avec l'anion et des exemplesIls sont basés sur la mesure du différentiel de potentiel électrique entre le pH de l'électrode et l'électrode de référence.
Le fonctionnement de ces mètres de pH est expliqué plus de profondeur dans la section suivante, mais en général, ces indicateurs sont considérés comme la normale la plus précise, fournissant un nombre précis (à la précision de 0,01 unités de pH) du paramètre et en comptant avec une sensibilité et vitesse supérieure aux deux autres méthodes.
De plus, d'autres caractéristiques, telles que les solides dissous, la conductivité électrique et la température de la solution peuvent également mesurer.
The only disadvantage of this type of pH meters is that they are delicate equipment and, in addition to an initial calibration that must perform an instrumentalist or connoisseur of the equipment, they will also need to be regularly cleaned to prevent the electrodes from suffering accumulation of matériel dans ces.
Comment fonctionnent les indicateurs de pH?
Indicateurs liquides
Les indicateurs liquides changent de couleur par protonation ou non-sens dans sa structure (selon la nature de base ou acide de l'indicateur), qui est basé sur l'équilibre de la réaction, comme suit: Hin + H2Ou ↔ h3SOIT+ + Dans-
Autrement dit, une fois l'indicateur ajouté à la solution, si l'équilibre de ce milieu commence à tendre à la direction opposée en augmentant ou en diminuant l'ion hydronium (encore une fois, en fonction de la nature de l'indicateur), cela changera de couleur jusqu'à Restez enfin dans une nouvelle couleur invariable.
Indicateurs
Les indicateurs, en particulier le papier décisif, doivent entrer en contact avec la solution à analyser discrètement pour pouvoir mesurer avec précision.
Peut vous servir: état liquideAutrement dit, dans une solution liquide, cela ne doit pas être introduit complètement, mais doit être dégoulinable ou toucher brièvement un échantillon de la substance.
Dans le cas d'une solution gazeuse, le gaz doit passer à la surface du papier pour permettre le contact et ce changement de couleur.
pH -metros
Les pH-metters fonctionnent par la différence électrique potentielle entre un pH et une électrode de référence.
Le pH-Meter mesure la tension qui existe entre deux électrodes dans une solution et montre le résultat converti en une valeur de pH correspondante.
L'équipement lui-même se compose de quelques électrodes - dont l'une est métallique et insensible au pH de la solution - et un simple amplificateur électronique. Pour son étalonnage, l'équipement est calibré avec des solutions de pH connues.

