Hexano (C6H14) Propriétés physiques et chimiques, structure, utilisations, toxicité
- 1016
- 166
- Adrien Remy
Il hexane Il s'agit d'un hydrocarbure qui se caractérise par un composé organique dont la formule chimique condensée est C est6H14. C'est un liquide transparent incolore et transparent, qui ne peut pas être mélangé avec de l'eau. Il présente cinq isomères, le linéaire étant l'un des hydrocarbures paraffiniques les plus importants de l'industrie et de la recherche.
L'hexane est obtenu par distillation fractionnée de l'huile brute. Il est également naturellement présent dans les agrumes et les fractions volatiles de diverses plantes ou fruits tels que la pomme, la goyave, les noisettes rôties, la patate douce et la sauge.
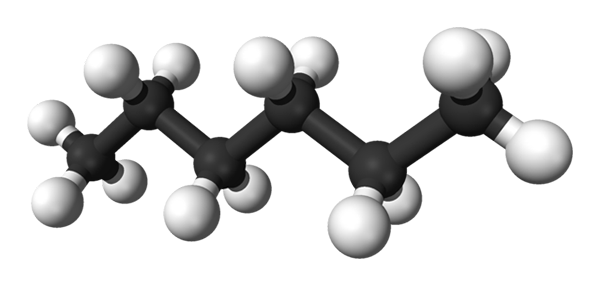
 Molécule n-hexane. Source: Benjah-Bmm27 [domaine public]
Molécule n-hexane. Source: Benjah-Bmm27 [domaine public] C'est un liquide volatil très inflammable que l'on trouve dans l'essence, la colle à séchage rapide et le ciment à frotter. L'hexane est utilisé comme solvant dans le processus d'extraction des huiles végétales, ainsi que des lipides et des graisses présentes dans les eaux et les sols contaminés.
Les personnes qui sont professionnellement exposées à l'hexano peuvent subir des dommages au système nerveux périphérique, manifesté par des picotements et des jambes dans les jambes et les bras; En plus de la faiblesse musculaire généralisée et, dans des cas graves, de l'atrophie des muscles squelettiques.
[TOC]
Propriétés physiques et chimiques des hexans
Apparence physique
Incolore, transparent et très volatile liquide.
Masse molaire
86 178 g / mol
Odeur
Essence similaire
Seuil d'odeur
1,5 ppm
Densité
0,6606 g / ml
Point de fusion
-96 à -94 ºC
Point d'ébullition
68,5 à 69,1 ºC
point d'allumage
-22 ºC (tasse fermée).
Solubilité dans l'eau
9,5 mg / L (pratiquement non miscible avec l'eau)
Solubilité dans les solvants
Très soluble dans l'éthanol, soluble dans l'éthyl éther et le chloroforme. Miscible avec de l'alcool, du chloroforme et de l'éther.
Densité relative de la vapeur avec l'air
2,97 (air = 1)
Coefficient de partition octanol / eau
Log p = 3 764
La pression de vapeur
17,60 kPa à 20 ºC
Longueur d'onde de la densité optique maximale
200 nm
Il peut vous servir: niobio (NB): structure, propriétés, utilisations, obtentionIndice de réfraction
1 375
Gelée
0,3 MPa · s
Capacité calorique
265.2 J · K-1· Mol-1
Chaleur de combustion
4.163.2 kJ · mol-1
Chaleur de vaporisation
31,56 kJ · mol-1
Tension superficielle
17,89 MN / m A 25 ºC
Potentiel d'ionisation
10,18 eV
La stabilité
Écurie. Incompatible avec les agents oxydants, le chlore, le fluor, le perchlorate de magnésium. Forme un mélange explosif avec l'air.
Réactivité
L'hexane peut réagir vigoureusement avec des matériaux oxydants, qui peuvent inclure du chlore liquide, de l'oxygène concentré, de l'hypochlorite de sodium et de l'hypochlorite de calcium. Il est également incompatible avec le tétroxyde de dyitroge. Hexane peut attaquer certaines formes de plastiques, de caoutchouc et de revêtements.
Structure d'hexane
Interactions intermoléculaires
La première image montre la molécule du n-Hexane représenté par un modèle de sphères et de barres. Les sphères noires correspondent à des atomes de carbone, composant le squelette de carbone en zigzag, tandis que les sphères blanches sont des atomes d'hydrogène. Il n-Hexano est donc un hydrocarbure, linéaire et très dynamique.
Parce que tous ses liens C-H sont une faible polarité, la molécule n'a pas le moment dipolaire. Ce faisant, ses interactions intermoléculaires ne sont pas du dipol-dipol.
Chaque molécule de n-Hexano "s'adapte" l'un sur l'autre à des températures très basses, comme il serait supposé dans sa structure cristalline. D'un autre côté, dans le liquide, leurs squelettes fléchissent et font pivoter leurs liaisons C-H, originaire de ce fluide est volatile et bouille à 68,7 ºC.
Isomères
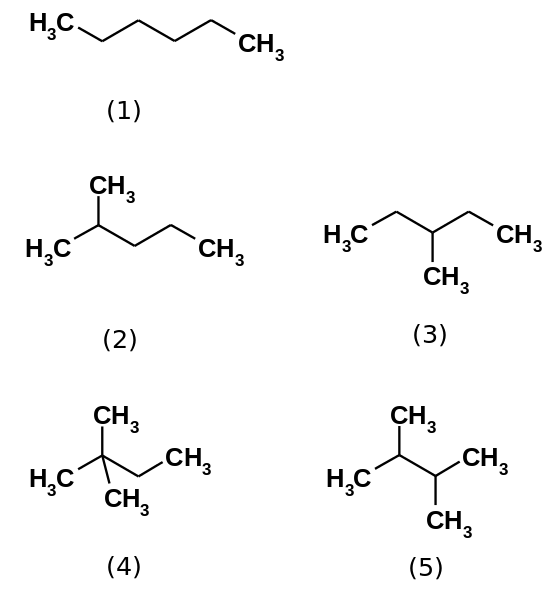 Les cinq isomères hexane. Source: Steffen 962 [domaine public]
Les cinq isomères hexane. Source: Steffen 962 [domaine public] Les hydrocarbures hexane se compose en fait de cinq isomères, étant le n-Hexane le moins ramifié, (1). Les quatre autres isomères sont, dans l'ordre croissant:
2-méthylpropane (2)
3-méthylpropane (3)
2,2-diméthylbutane (4)
2,3-diméthylbutane (5)
Notez que les structures deviennent plus ramifiées de (1) à (5). Étant plus ramifiés, les forces dispersives diminuent, car il n'y a plus de portions linéaires qui guérissent efficacement. Cela conduit à une diminution et une variation des points d'ébullition des isomères; Bien que certaines écarts acceptables soient observés.
Peut vous servir: quel est l'erristeneo?Les deux 2-méthylpropane. Ensuite, il est suivi du 2,3-diméthylbutane (PEB = 58 ºC), pour enfin placer le 2,2-diméthylbutane comme liquide le plus volatil (PEB = 49,7 ºC).
Applications
L'hexane est mélangé à des produits chimiques similaires pour produire des solvants. Parmi les noms que ces solvants reçoivent figurent l'hexane commercial, les hexans mixtes, etc. Ils sont utilisés comme agents de nettoyage dans l'industrie textile, les meubles et l'impression creux.
Hexane est un ingrédient de la colle utilisée dans l'étanchéité des toits, dans les chaussures et le cuir. Il est également utilisé pour lier les livres, mouler les pilules et les comprimés, rincer, faire des pneus et des balles de baseball.
L'hexane est utilisé pour déterminer l'indice de réfraction minérale et le liquide de remplissage pour les thermomètres au lieu du mercure; Généralement avec une teinture rouge ou bleue. Il est également utilisé dans l'extraction de l'huile de graisse et d'eau pour l'analyse de ses polluants.
Hexano est utilisé comme solvant dans l'extraction de l'huile de graines végétales, comme le soja, le canola ou le bit. De plus, il est utilisé pour dégraisser des morceaux d'origine différentes. Il est utilisé dans la dénaturation de l'alcool, dans la méthode d'analyse HPLC et la spectrophotométrie.
Toxicité
Inhalation et contact
La toxicité aiguë de l'hexane est relativement faible, bien qu'il s'agisse d'un anesthésique léger. Une exposition aiguë à des concentrations élevées d'hexane peut produire par inhalation, une légère dépression du système nerveux central (SNC), qui se manifeste par des étourdissements, des vertiges, des nausées légères et des maux de tête.
Peut vous servir: réaction endothermiqueIl peut également provoquer la dermatite et l'irritation des yeux et de la gorge. L'inhalation chronique de l'hexane, liée à l'activité de travail, peut endommager le système nerveux périphérique (Sensomotor Polyneuropathie).
Les premiers symptômes sont des picotements et des crampes et bras de jambe, suivis d'une faiblesse musculaire. Dans les cas graves, il peut y avoir une atrophie des muscles squelettiques, ainsi que la perte de coordination et les problèmes de vision.
La toxicité de l'hexane est liée à la génération du métabolite hexane-2,5-diona. Cela réagit avec la lysine d'acide aminé d'une chaîne latérale protéique, produisant la perte de la fonction protéique.
Dose de sécurité
L'Agence de protection de l'environnement (EPA) a calculé une concentration de référence (RFC) pour l'hexane de 0,2 mg / m3, et une dose de référence (RFD) de 0,06 mg / kg de poids / jour.
Dans les années 1960 et 1970, la présence d'altérations nerveuses. La cause était qu'ils ont inspiré une atmosphère d'hexane de 500 - 2.500 ppm, pour 8 à 14 heures par jour.
Les travailleurs ont présenté les symptômes connus de l'inhalation chronique de l'hexano, découvrant les médecins que les nerfs qui contrôlaient les muscles des bras et des jambes étaient endommagés.
Les références
- Danielle Reid. (2019). Hexane: structure, formule et propriétés. Étude. Récupéré de: étudier.com
- Centre national d'information sur la biotechnologie. (2019). Hexane. Base de données PubChem. CID = 8058. Récupéré de: pubchem.NCBI.NLM.NIH.Gouvernement
- Wikipédia. (2019). Hexane. Récupéré de: dans.Wikipédia.org
- Monde des molécules. (s.F.). Molécule d'hexane. Récupéré de: WorldofMolecules.com
- Livre chimique. (2017). Hexane. Récupéré de: Chemicalbook.com
- Le Commonwealth d'Australie. (s.F.). N-hexane: sources de problèmes. Récupéré de: npi.Gouvernement.Au
- EPA. (2000). Hexane. [PDF]. Récupéré de: EPA.Gouvernement
- Agence pour le registre des substances toxiques et des maladies. (1999). Énoncé de santé Pub Pub pour N-hexan. Récupéré de: ATSDR.CDC.Gouvernement
- « 5 expériences de réactions chimiques (simple et sûre)
- Caractéristiques de Toronjil, habitat, propriétés, culture, soins »

