Structure cristalline
- 4795
- 1076
- Prof Ines Gaillard
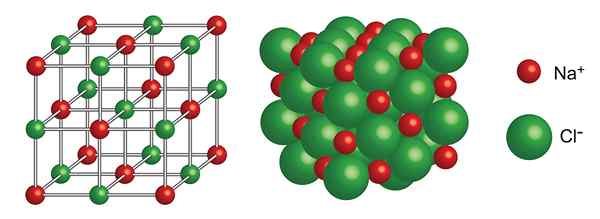
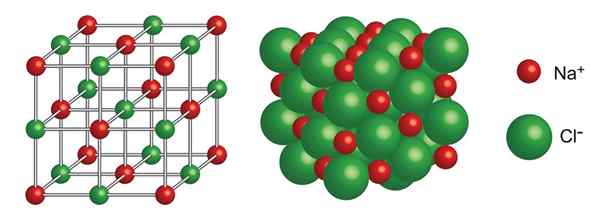 Structure cristalline du chlorure de sodium
Structure cristalline du chlorure de sodium Quelle est la structure cristalline?
La structure cristalline Il se réfère à la manière dont les atomes, les ions ou les molécules sont organisés ou emballés dans des solides cristallins tels que les diamants, le sel (chlorure de sodium) ou le sucre (saccharose).
Les solides cristallins se forment des réseaux à trois dimensions d'unités identiques appelées cellules unitaires. Ceux-ci ressemblent à de petits blocs de construction identiques (tels que les Layos) qui se lient les uns aux autres pour former les cristaux que nous pouvons voir à l'œil nu.
La structure cristalline se compose d'une description de la forme de cette cellule unitaire et de la position exacte de chaque atome dans ladite cellule.
Caractéristiques de la structure cristalline
Sont formés par des cellules unitaires qui sont répétées
La structure cristalline consiste en la répétition d'une cellule unitaire dans toutes les directions. Ces cellules sont constituées de parallélépipés à trois dimensions dont la forme et la taille sont définies par trois vecteurs appelés un B et c, et par les angles entre ces vecteurs, appelés α, β et γ.
Ce sont des structures hautement ordonnées
La structure cristalline se caractérise par l'un des états les plus ordonnés qui existent. Les cristaux sont ainsi ordonnés qu'avec une connaissance de la structure de la cellule unitaire qui ne contient qu'une poignée d'atomes, toute la structure d'un verre formé par des millions d'atomes, d'ions ou de molécules peut être reconstruite.
Ils présentent une symétrie
La plupart des cellules unitaires avec lesquelles des solides cristallins peuvent être construits ont un certain type de symétrie. Cela signifie que le contenu d'une partie de la cellule est répété dans une autre partie de celui-ci après avoir effectué une rotation, une réflexion ou un investissement.
Peut vous servir: séchoir rotatif: fonctionnement, à quoi sert-il, pièces, applicationsPar exemple, si une cellule unitaire a un plan de symétrie, cela signifie que la moitié de la cellule est le reflet de l'autre.
Relation entre les propriétés de la matière et la structure cristalline
Il existe de nombreuses propriétés physiques et chimiques qui dépendent de la structure cristalline:
Densité
Selon la façon dont les atomes sont emballés dans la structure cristalline, des structures ou des structures plus compactes peuvent être obtenues dans lesquelles les atomes sont plus éloignés les uns des autres. Dans le premier cas, un solide dense et lourd sera obtenu, car plus d'atomes sont emballés dans un volume inférieur.
-
Exemple
Si nous comparons les trois structures cristallines cubes appelées simples cubes (P), centrées cubes sur les faces (FCC) et centrées cubes sur le corps (BCC) pour les atomes égaux, la structure BCC est 2 est 2.6 fois plus dense que la FCC, et la FCC est 1.4 fois plus dense que P.
Forme cristalline
La forme des cristaux que nous pouvons voir à l'œil nu est le reflet de la structure cristalline, et en particulier de la cellule unitaire. Selon la structure de la cellule unitaire, les cristaux grandiront plus dans une direction que dans d'autres, ce qui donne naissance à des cristaux avec différentes formes telles que les aiguilles, les quotas, les cristaux hexagonaux, etc.
Anisotropie
Les propriétés physiques telles que la conductivité thermique ou électrique et les propriétés magnétiques de la matière sont souvent plus importantes dans une direction du matériau que tout au long d'un autre.
C'est ce qu'on appelle l'anisotropie, et ces effets sont particulièrement intenses dans les structures cristallines car ce sont des structures très ordonnées et régulières.
Peut vous servir: diastréomèresTypes de structure cristalline
Les structures cristallines peuvent être classées en fonction du type de cellule unitaire par laquelle elles sont formées. Ceux-ci sont caractérisés par les trois côtés qui se connectent à l'un de ses bords (appelés a, b et c) et par les angles entre ces côtés (appelés α, β et γ).
Cela donne naissance à 7 systèmes cristallins. Dans chacun de ces systèmes cristallins, différents types de cellules unitaires peuvent être distingués. Au total, il existe 14 cellules unitaires différentes qui sont appelées réseaux Bravais et sont représentés ci-dessous:
Système cube
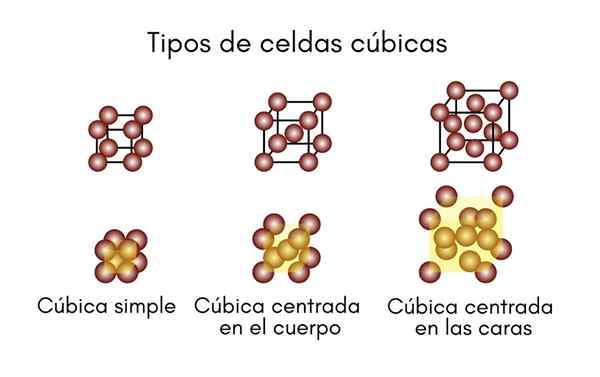
Comme son nom l'indique, la cellule unitaire se compose d'un cube parfait. Les trois côtés, A, B et C sont égaux les uns aux autres, et leurs trois angles sont tous à 90 °. Ce système se compose de cellules:
- Cubique simple ou primitif.
- Centré cube dans le corps (BCC).
- Coube centré sur les visages (FCC).
Système tétragonal
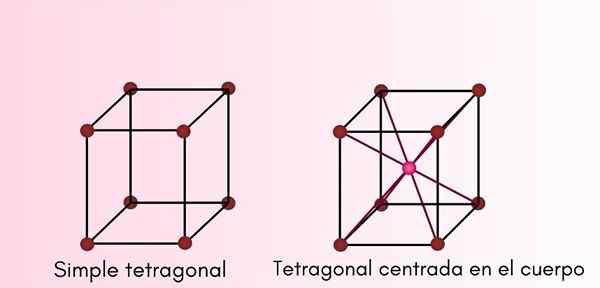
Dans ce type de structure cristalline, A et B sont les mêmes, mais C est différent, mais tous restent perpendiculaires les uns aux autres. Les cellules tétragonales peuvent être:
- Tétragonal simple ou primitif.
- Tétragonal centré sur le corps.
Système Ortorrombique
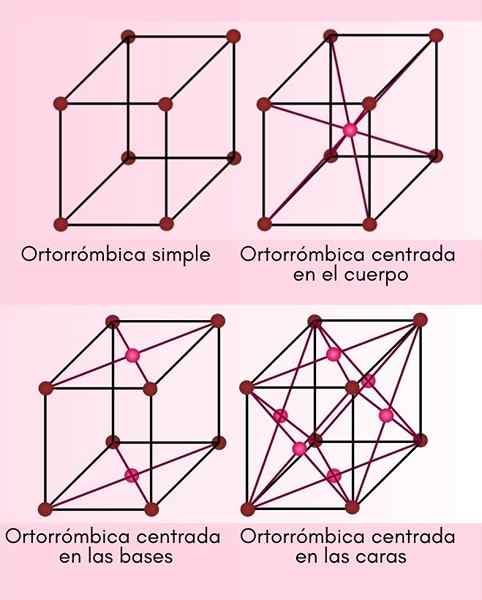
Dans ce système cristallin, A, B et C sont tous différents, mais ils sont toujours perpendiculaires les uns aux autres. Il y a 4 cellules ortorrombiques différentes:
- Ortorrombique primitif ou simple.
- Orthrome centré sur le corps.
- Orthrome centré sur la base.
- Ortorombique centré sur le visage.
Système monoclinique
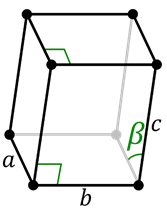 Cellule monoclinique primitive
Cellule monoclinique primitive 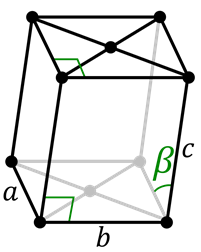 Cellule monoclinique concentrée sur la base
Cellule monoclinique concentrée sur la base Le système monoclinique est similaire à l'hexagonal, à l'exception du fait que tous ses côtés sont différents. Il y a deux cellules pour le système monoclinique:
- Monoclinique primitif.
- Monoclinique centré sur la base.
Système triclinique
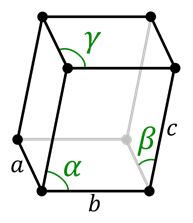 Cellule triclinique
Cellule triclinique Dans le système de tricyclage, il n'y a pas de symétrie. Tous les angles sont différents les uns des autres et ne doivent pas nécessairement être à 90 °. Tous ses côtés sont également différents.
Système hexagonal
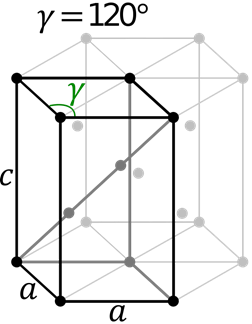 Cellule hexagonale
Cellule hexagonale Cette cellule contient les côtés A et B du côté C différent et différent. Les angles α et β sont à 90 ° tandis que γ = 120 °.
Système trigonal ou rhomboyan
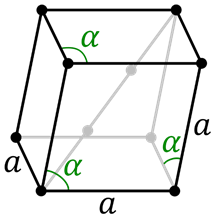 Cellule trigonale ou rhomboédicale
Cellule trigonale ou rhomboédicale Il s'agit d'un type particulier de structure similaire à la prise d'un seau et à l'étirer le long de deux sommets opposés. Tous les côtés sont les mêmes et aussi leurs angles, mais ce ne sont pas à 90 °.
Exemples de structures cristallines
Chlorure de sodium
Sa structure cristalline se compose d'un réseau cube centré sur des visages avec 4 unités NaCl pour chaque cellule unitaire,
Fer alfa
Le fer cristallise le fer alpha à 768 ° C. Sa structure est centrée cubique dans le corps avec un 2e bord de 2.86 Å (ou 286 pm)
Fer gamma
Il s'agit d'une forme de fer qui se produit entre 910 ° C et 1400 ° C et a une structure cristalline cubique centrée sur les faces de 3.64 Å (364 pm) de bord.
diamant
Le diamant est l'une des formes de carbone les plus précieuses et a une structure cristalline cubique centrée sur les faces (FCC) qui contient deux atomes de carbone et un bord de 3 de 3.75 Å (375 pm).
Graphite
Le graphite est un autre carbone très commun. Dans ce cas, ce sont des feuilles d'atomes de carbone ensemble formant ensemble des anneaux de 6 ans, qui donnent naissance à une structure cristalline hexagonale.

