Lien d'ester
- 2530
- 629
- Anaïs Julien
Qu'est-ce qu'un lien d'ester?
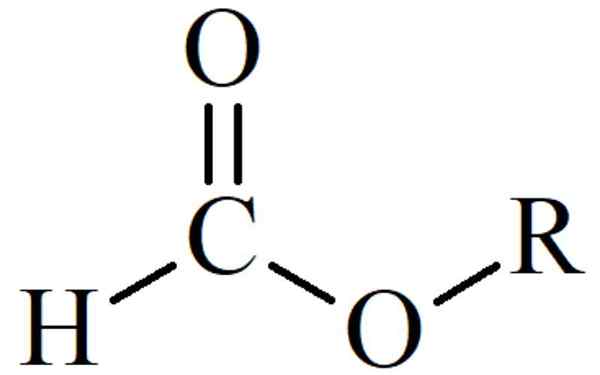
UN Lien d'ester Il s'agit d'un lien entre un groupe d'alcool (-OH) et un groupe d'acide carboxylique (-COOH), formé par l'élimination d'une molécule d'eau (H₂O).
La figure 1 montre la structure de l'acétate d'éthyle. La liaison ester est la simple liaison qui se forme entre l'oxygène de l'acide carboxylique et le carbone d'éthanol.
R-COOH + R'-OH → R-COO-R '+ H₂O
Dans la figure, la zone bleue correspond à la partie du composé qui provient de l'éthanol et de la zone jaune de l'acide acétique.
Hydrolyse des liens d'ester
Pour comprendre un peu mieux la nature des liaisons d'ester, le mécanisme de réaction d'hydrolyse de ces composés est expliqué.
Le lien d'ester est relativement faible. En milieu acide ou basique, il est hydrolysé pour former respectivement l'alcool et l'acide carboxylique. Le mécanisme de réaction d'hydrolyse des esters est bien étudié.
Dans un milieu de base, les premiers hydroxydes nucléophiles attaquent dans le C électrophile de l'ester C = O, rompant le lien π et créant l'intermédiaire tétraédrique.
Ensuite, l'intermédiaire s'effondre, réformant le C = O et entraînant la perte du groupe sortant, l'alcoxyde, Ro-, qui conduit à l'acide carboxylique.
Enfin, une réaction acide / base est un équilibre très rapide, où l'alcoxyde, Roworks comme base qui déprotons l'acide carboxylique, RCO2H (un traitement acide permettrait à l'acide carboxylique d'être obtenu à partir de la réaction).
Le mécanisme de l'hydrolyse de la liaison d'ester dans le milieu acide est un peu plus compliqué. Une réaction acide / base se produit, et comme seulement un nucléophile faible et un mauvais électrophile.
La protonation de l'ester carbonyle le rend plus électrophylique. Dans la deuxième étape, l'oxygène de l'eau fonctionne comme le nucléophile, attaquant le C électrophylique dans le C = O, les électrons se déplaçant vers l'ion hydronium, créant l'intermédiaire tétraédrique.
Dans la troisième étape, une réaction acide / base se produit par l'oxygène qui provenait de la molécule d'eau pour neutraliser la charge.
Dans la quatrième étape, une autre réaction acide / base se produit. Le -och3 doit être fait, mais il est nécessaire de devenir un bon groupe sortant pour la protonation.
Peut vous servir: masse: concept, propriétés, exemples, calculDans la cinquième étape, les électrons d'un oxygène adjacent sont utilisés pour aider à «expulser» le groupe sortant, produisant une molécule neutre d'alcool.
Dans la dernière étape, une réaction acide / base se produit. La non-témoignage de l'ion hydronium révèle le carbonyle c = o dans le produit carboxylique acide et régénère le catalyseur acide.
Types de liens d'ester
Ester carbonique
Les esters de charbon sont les plus courants de ce type de composé. Le premier ester carbonique était l'acétate d'éthyle, également appelé éthanoate d'éthyle.
Autrefois, ce composé était connu sous le nom d'éther de vinaigre. De son nom en allemand, Essig-autre, Il a dérivé le nom de ce type de composés.
Les esters se trouvent dans la nature et sont largement utilisés dans l'industrie. De nombreux esters ont des odeurs de fruits caractéristiques, et beaucoup sont naturellement présents dans les huiles essentielles des plantes.
Cela a également conduit à une utilisation courante dans les arômes et les parfums artificiels lorsqu'il s'agit d'imiter les odeurs.
Plusieurs milliards de kilogrammes de polyesters sont produits industriellement, des produits importants tels que le téréphtalate de polyéthylène, l'acrylate et les esters d'acétate de cellulose.
Le lien d'ester des esters carboxyliques est responsable de la formation de triglycérides dans les organismes vivants.
Les triglycérides se trouvent dans toutes les cellules, mais principalement dans le tissu adipeux, ils sont la principale réserve d'énergie que le corps a.
Les tricilglycérides (TAG) constituent des molécules de glycérol liées à trois acides gras au moyen d'une liaison ester. Les acides gras présents dans l'étiquette sont principalement saturés.
Les triacylglycérides (triglycérides) sont synthétisés pratiquement dans toutes les cellules. Les principaux tissus de la synthèse de Tag sont l'intestin grêle, le foie et les adipocytes. À l'exception de l'intestin et des adipocytes, la synthèse des tags commence par le glycérol.
Le glycérol est d'abord phosphorylé avec la chette de glycérol, puis les acides gras activés (acide gras-coas) servent de substrats pour l'ajout d'acides gras qui génèrent de l'acide phosphatidique. Le groupe phosphate est séparé et le dernier acide gras est ajouté.
Dans l'intestin grêle, les étiquettes alimentaires sont hydrolysées pour libérer les acides gras et les monoacylglycérides (MAG) avant la capture par les entérocytes. Les entérocytes MAS servent de substrats d'acallation dans un processus à deux étages produit par une balise.
Peut vous servir: état liquideDans le tissu adipeux, il n'y a pas d'expression de kinase glycérol, de sorte que le bloc de construction pour TAG dans ce tissu est l'intermédiaire glycolytique, le phosphate de dihydroxyacétone, DHAP.
Le DHAP est réduit au glycérol-3-phosphate par le glycérol-3-phosphate cytosolique déshydrogénase et la réaction restante de la synthèse de TAG est la même que pour tous les autres tissus.
Ester phosphorique
Les esters phosphoriques sont produits par la formation d'une liaison d'ester entre l'alcool et l'acide phosphorique. Compte tenu de la structure acide, ces esters peuvent être mono, di et trisusuidos.
Ce type de liaisons d'ester se trouve dans des composés tels que les phospholipides, l'ATP, l'ADN et l'ARN.
Les phospholipides sont synthétisés par la formation d'une liaison d'ester entre l'alcool et le phosphate d'acide phosphatique (1,2-diacylglycérol 3-phosphate). La plupart des phospholipides ont un acide gras saturé sur C-1 et un acide gras insaturé sur C-2 du squelette de glycérol.
Les alcools les plus couramment ajoutés (sérine, éthanolamine et colline) contiennent également de l'azote qui peut être chargé positivement, tandis que le glycérol et l'inositol ne sont pas.
L'adénosyntrifosphate (ATP) est une molécule qui est utilisée comme monnaie énergétique dans la cellule. Cette molécule est composée d'une molécule d'adénine attachée à la molécule ribose à trois groupes de phosphate.
Les trois groupes de phosphate de la molécule sont appelés gamma (γ), bêta (β) et alpha (α), ce dernier estérifie le groupe hydroxyle C-5 du ribose.
Le lien entre le ribose et le groupe α-phosphoryle est une liaison phosphoester car elle comprend un atome de carbone et un atome de phosphore, tandis que les groupes β et γ-phosphoryle dans l'ATP sont connectés par des liaisons phosphoandites.
Tous les phosphoanhydros ont une énergie chimique considérable, et l'ATP ne fait pas exception. Cette énergie potentielle peut être utilisée directement dans les réactions biochimiques.
Une liaison phosphodiéster est une liaison covalente dans laquelle un groupe phosphate se lie aux carbones adjacents via des liaisons d'ester. Le lien est le résultat d'une réaction de condensation entre un groupe hydroxyle de deux groupes de sucre et un groupe phosphate.
Peut vous servir: lien covalent coordonnéLa liaison de la diète entre l'acide phosphorique et deux molécules de sucre dans l'ADN et l'ARN squelette relie deux nucléotides ensemble pour former des polymères oligonucléotidiques. La liaison phosphodiéster relie un carbone de 3 'avec un carbone 5' dans l'ADN et l'ARN.
(Base1) - (ribosa) -oh + ho -p (o) 2 -o- (ribosa) - (base 2)
(Base1) - (ribosa) - o - p (o) 2 - o- (ribosa) - (base 2) + h₂o
Au cours de la réaction de deux des groupes hydroxyles dans l'acide phosphorique avec un groupe hydroxyle dans deux autres molécules, deux liaisons ester sont formées dans un groupe phosphodiéster. Une réaction de condensation dans laquelle une molécule d'eau est perdue génère chaque lien d'ester.
Pendant la polymérisation nucléotidique pour former des acides nucléiques, le groupe hydroxyle du groupe phosphate se lie au carbone 3 'd'un sucre nucléotidique pour former une liaison ester au phosphate d'un autre nucléotide.
La réaction forme une liaison phosphodiéster et élimine une molécule d'eau.
Ester sulfurique
Les esters sulfuriques, ou thioés, sont composés du groupe fonctionnel R-S-CO-R. Ils sont le produit de la stérification entre un acide carboxylique et un thiol ou avec de l'acide sulfurique.
En biochimie, les gars les plus connus sont dérivés de Coenzyme A, par exemple, l'acétyl-CoA.
L'acétyl coenzyme A ou l'acétyl-CoA est une molécule qui participe à de nombreuses réactions biochimiques. Il s'agit d'une molécule centrale dans le métabolisme des lipides, des protéines et des glucides.
Sa fonction principale est de livrer le groupe acétyle au cycle d'acide citrique (cycle de Krebs) qui sera oxydé pour la production d'énergie. C'est aussi la molécule précurseur de la synthèse des acides gras et est un produit de la dégradation de certains acides aminés.
Les acides gras activés par COA mentionnés ci-dessus sont d'autres exemples de thioésters qui proviennent de la cellule musculaire. L'oxydation des ucioners d'acide gras-CoA se produit vraiment dans les corps vésiculaires discrets appelés mitochondries.
Les références
- Organosulfure composé. Récupéré de Britannica.com.
- Hydrolyse des ESER. Chem récupéré.Ucalgaire.CA.
- Obligation d'ester. Récupéré des sciences futures.nous.

