Énantiomères
- 3554
- 191
- Noa Da silva
Nous expliquons quels énantiomères et chiralité, leurs propriétés, la nomenclature et plusieurs exemples sont
 Ces deux composés sont des énantiomères, car ils sont formés par les mêmes atomes, unis de la même manière et sont des images spéculaires les unes des autres
Ces deux composés sont des énantiomères, car ils sont formés par les mêmes atomes, unis de la même manière et sont des images spéculaires les unes des autres Quels sont les énantiomères?
Les énantiomères Ce sont des paires de composés qui sont des images miroir non overlampables les unes des autres. Ces paires de composés sont un type particulier d'isomères, c'est-à-dire que ce sont des composés différents qui ont la même formule moléculaire.
Il existe différents types d'isomères parmi lesquels sont des stéréoisomères, dans lesquels tous les atomes sont unis dans le même ordre et avec le même type de liens, mais ils ont des orientations différentes dans l'espace (stéréo signifie espace).
Dans les stéréoisomères, nous trouvons les énantiomères, dont la caractéristique principale est d'être des images spéculaires les unes avec les autres.
Les énantiomères sont de nature très courante. En fait, presque tous les composés organiques présents dans les cellules de tous les êtres vivants sont l'un des deux énantiomères possibles.
Par exemple, tous les acides aminés qui font partie des protéines naturelles correspondent à l'énantiomère L de l'acide aminé respectif (l'autre isomère s'identifie à la lettre D).
D'un autre côté, les ingrédients actifs de la grande majorité des médicaments existent également sous forme de paires d'énantiomères, dont un seul est efficace. La difficulté de séparer les énantiomères les uns des autres signifie que les médicaments qui ne contiennent que l'isomère utile sont très chers.
Énantiomères et chiralité
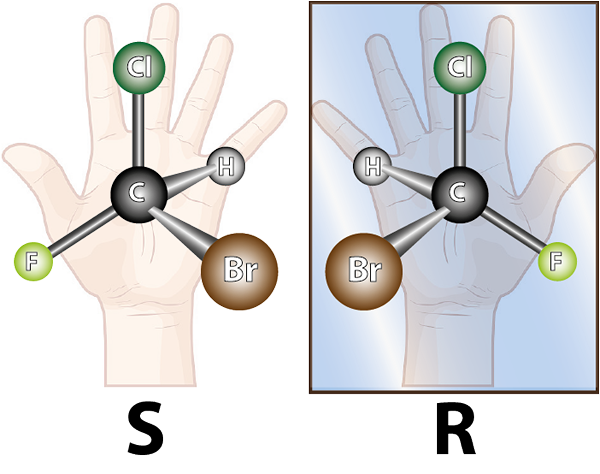
Les énantiomères sont formés par des molécules chirales. La chiralité est la propriété de ne pas être chevauché avec son image miroir. Le mot chiral vient du terme grec, Kheir Ce qui signifie la main, se souvenant du fait que les mains sont également des images spéculaires les unes des autres, et elles ne peuvent pas se chevaucher.
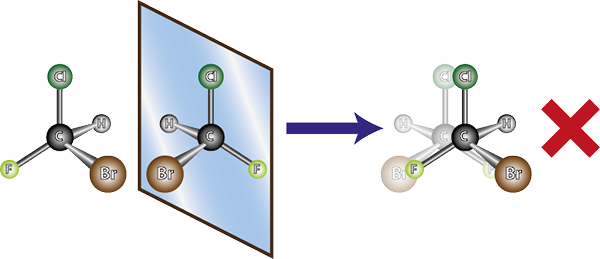 La molécule de la gauche est chirale, car lors de la comparaison avec son image miroir, on peut voir qu'ils ne se chevauchent pas. En d'autres termes, il n'y a aucun moyen de tourner ou de le tourner de telle manière que tous les atomes coïncident les uns avec les autres
La molécule de la gauche est chirale, car lors de la comparaison avec son image miroir, on peut voir qu'ils ne se chevauchent pas. En d'autres termes, il n'y a aucun moyen de tourner ou de le tourner de telle manière que tous les atomes coïncident les uns avec les autres Compte tenu de ce qui précède, il peut être déduit que pour chaque molécule chirale, il doit y avoir une autre molécule chirale qui n'est pas une image miroir qui ne se chevauchent pas, c'est-à-dire son énantiomère. En d'autres termes, chaque fois qu'une molécule est dite.
Peut vous servir: néodyme: structure, propriétés, utilisationsCentres chiraux
De nombreux composés chiraux ont un ou plusieurs centres asymétriques responsables de la chiralité de la molécule. Ceux-ci sont appelés centres chiraux et dans de nombreux composés organiques sont constitués d'atomes de carbone liés à 4 atomes ou groupes d'atomes différents.
La forme particulière à mesure que ces quatre groupes sont distribués autour du carbone asymétrique détermine lequel des deux énantiomères correspond à une molécule chirale. La présence d'un seul centre quiral garantit que la molécule est chirale, mais s'il y en a plusieurs, elle peut être chirale car elle peut ne pas.
Propriétés de l'éontiomère
La plupart des propriétés physiques et chimiques sont identiques
Comme la main droite et la main gauche, les énantiomères ne viennent qu'en paires. Ces composés sont pratiquement identiques les uns aux autres. En fait, la plupart de ses propriétés physiques et chimiques telles que le point de fusion, d'ébullition, de pression de vapeur et de solubilité dans certains solvants, entre autres, sont identiques.
Activité optique
Tous les composés chiraux ont une propriété unique qui les distingue de ceux qui ne le sont pas: ils ont la capacité de faire tourner le plan de la lumière polarisée. Cette propriété est appelée Activité optique, Et c'est l'une des rares propriétés qui distingue un composé chiral de son énantiomère.
Ce dernier est dû au fait que le plan lumineux polarisé peut être tourné dans l'une des deux directions, soit dans le sens des aiguilles d'horloge (appelés dextrogyr et représentés avec le symbole +) ou contre les aiguilles de l'horloge (Levógiro, représentée avec le symbole -).
Si un composé étrange tourne le plan lumineux polarisé dans une direction, son énantiomère le tourne dans la direction opposée.
-
Exemple
Une solution de D-glucosa tourne le plan de lumière polarisé dans la direction des aiguilles de l'horloge (vers la droite, c'est dextrogyral), tandis qu'une solution de glycose en L le fait tourner dans la direction opposée.
Il peut vous servir: Erlenmeyer Flask: caractéristiques, utilisations, méthodes d'utilisationRéactivité différentielle
Une autre propriété qui permet de distinguer l'une desantión de l'autre, est sa réactivité contre d'autres composés chiraux.
La réactivité différentielle peut être comparée à la façon dont un gant ne semble bien que d'une part, mais pas à l'autre, ou en tant que chaussure droite s'adapte bien au pied droit, mais pas à gauche.
Une conséquence importante de la réactivité différentielle est les différents effets qui peuvent provoquer les deux énantiomères de certains médicaments. Ces différences peuvent être inoffensives, mais elles peuvent également être très dangereuses.
-
Exemples
- Des deux énantimers de l'aspartame (qui est un édulcorant artificiel), l'un est sucré tandis que l'autre n'a pas de saveur.
- Seuls les énantiomères de l'oméprazole sont efficaces en tant que protecteur gastrique tandis que l'autre ne produit aucun effet.
- La D-pénicilamine est un médicament contre la polyarthrite rhumatoïde, tandis que son énantiomère, la L-pénicilamine est un poison dangereux.
Absorption différentielle
Les énantiomères diffèrent également dans la façon dont ils sont absorbés dans les résines ou les solides qui sont également des chiraux. Un mélange d'énantiomères peut être séparé s'il passe par une colonne de séparation chirale, car l'un des deux énantiomères sera absorbé plus fortement que l'autre.
Nomenclature des énantiomères
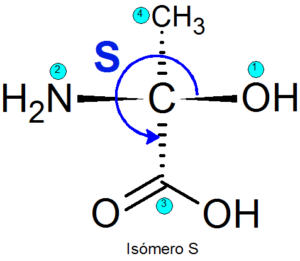
Il existe plusieurs méthodes pour identifier l'un ou l'autre énantiomère, mais le plus utilisé est le système Cahn-Ingold-Prelog (CIP). Cela se compose des étapes suivantes:
- Un niveau de hiérarchie est attribué aux quatre groupes attachés à chaque centre chiral. La priorité des groupes est attribuée en fonction du numéro atomique de l'atome directement lié au centre quiral. S'il y a deux atomes égaux, les nombres atomiques des atomes liés au premier sont ajoutés pour ajouter les nombres atomiques.
- La direction dans laquelle les trois groupes prioritaires sont voyagés lorsque les points de priorité les plus bas sont déterminés.
- Si la direction de l'itinéraire est dans le sens des mains de l'horloge, la configuration est attribuée R, Sinon, la configuration est attribuée S.
Exemple
Exemples d'énantiomères
D-glycéraldéhyde et l-glycéraldéhyde
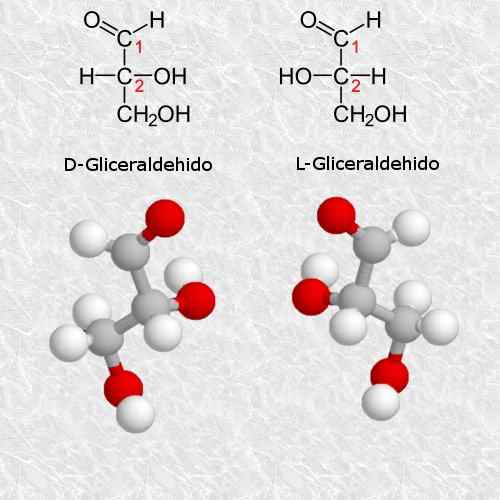
Le glycéraldéhyde est le glucides qui existent les plus simples et les plus petits qui existent, et est très important pour la chimie et la biologie.
Selon les règles du système CAHN-ingold-prélog, l'isomère D correspond à l'isomère (R) et l'isomère L correspond aux (s) (s) (s) (s).
D-Alanina et L-Alanina
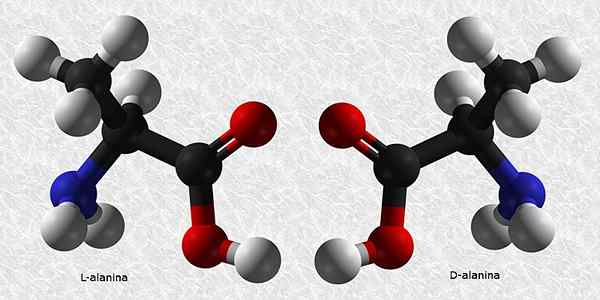
L'alanine est l'un des acides aminés essentiels pour la construction de protéines. Comme presque tous les acides aminés, il a un carbone chiral, il a donc deux énantiomères:
De ces deux, la L-Alanina est la plus courante et est présente dans tous les êtres vivants, tandis que la D-Alanina n'est présente que dans certaines parois cellulaires bactériennes.
Acide d-tartarique et l-tartarique
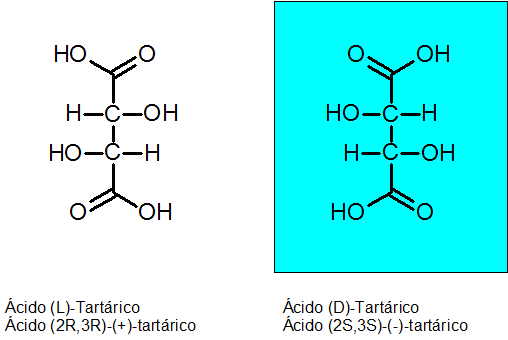
La chiralité a été découverte par Louis Pasteur en 1848 grâce à l'acide tartrique. Ce composé a 2 carbones asymétriques et peut exister sous forme de deux énantiomères plus un troisième isomère appelé Meso Compound.
La configuration absolue des deux carbones chiraux est R pour l'Enantiómero Levógiro et S pour l'énantiom dextrogyan.
2-butanol
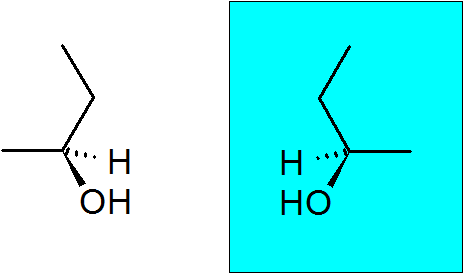
Cet alcool a également un carbone.
Bromocloroétan
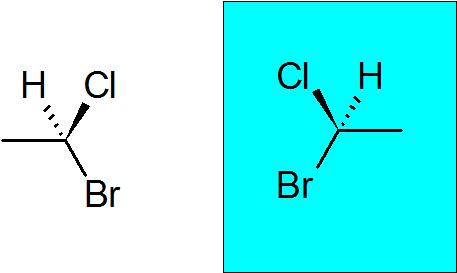
C'est un composé chiral très simple avec seulement deux carbones. Le carbone quantial a rejoint un brome, un chlore, un méthyle et un hydrogène.
Les références
- Chiralité (chimie). (18 mars 2021), sur Wikipedia.com
- Carey, F. POUR. (2008). Chimie organique. Boston: McGraw-Hill Higher Education.
- Smith, M., March, J., & March, J. (2001). La chimie organique avancée de mars: réactions, mécanismes et étendus. New York: Wiley.
- M.H. Hyun (2012). 8.13 séparations et analyses chromatographiques: phases chirales à base de la couronne chirale à base d'éther de la couronne. Éditeur (s): Erick M. Carreira, Hisashi Yamamoto. Comprendre la chiralité. Elsevier. Pages 263-285. ISBN 9780080951683,
- Nguyen, L. POUR., Il h., & Pham-Huy, C. (2006). Drogues chirales: un aperçu. Journal international des sciences biomédicales: IJBS, 2(2), 85-100.

