Structure de la capsule Bowman, histologie, fonctions
- 3689
- 728
- Raphaël Meyer
La Capsule à bowman Il représente le segment initial de la composante tubulaire du néphron, l'unité anátomo fonctionnelle du rein dans lequel les processus destinés à la production d'urine sont effectués et avec lesquels le rein contribue à la conservation de l'homéostasie de l'organisme.
Il a été nommé en l'honneur de l'ophtalmologiste anglais et docteur anatomiste Sir William Bowman, qui a découvert son existence et publié sa description histologique pour la première fois en 1842.
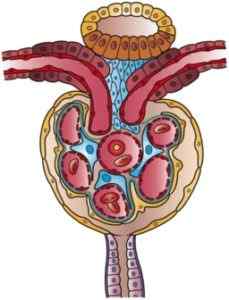 Illustration d'un néphron (source: œuvre d'art de Holly Fischer [CC par 3.0 (https: // CreativeCommons.Org / licences / par / 3.0)] via Wikimedia Commons)
Illustration d'un néphron (source: œuvre d'art de Holly Fischer [CC par 3.0 (https: // CreativeCommons.Org / licences / par / 3.0)] via Wikimedia Commons) Il y a une certaine confusion dans la littérature par rapport à la nomenclature des segments initiaux du néphron, parmi lesquels la capsule Bowman est incluse. Parfois, il est décrit comme une partie différente du glomérule et constituant avec lui le corpuscule rénal, tandis que pour d'autres, il a fonction en tant que membre du glomérule.
Indépendamment du fait que dans les descriptions anatomiques, la capsule fait partie du glomérule, le fait est que les deux éléments sont si intimement associés à sa structure et à sa fonction, que le terme glomérule se réveille qui pense à l'idée d'une sphérite avec son son navires.
Sinon, la capsule serait simplement un réceptacle dans lequel le fluide filtré dans le glomérule est versé, mais il n'aurait pas de partie dans le même processus de filtration glomérulaire. Ce qui n'est pas le cas, car elle, comme on le verra, fait partie de ce processus auquel elle contribue d'une manière spéciale.
[TOC]
Structure et histologie
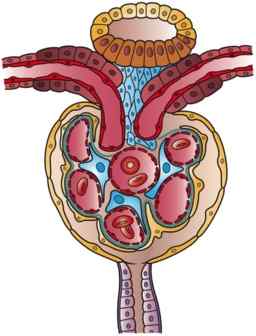
La capsule de Bowman est comme une petite sphère dont le mur est invaginé dans le secteur vasculaire. Dans cette invagination, la capsule est pénétrée par la collation capillaire, qui provient de l'artériola afférente et qui apporte du sang au glomérule, où l'eferent arteriola qui prend le sang du glomérule.
L'extrémité opposée de la capsule, appelée pôle urinaire, est présentée comme si la paroi de la sphère avait un trou auquel l'extrémité du premier segment qui commence la fonction tubulaire elle-même, c'est-à-dire le tubule à contour proximal est connecté.
Cette paroi externe de la capsule est un épithélium plat et est appelé l'épithélium pariétal de la capsule Bowman. Changer la structure lors de la transition vers l'épithélium du tubule proximal dans le pôle urinaire et vers l'épithélium viscéral dans le pôle vasculaire.
Peut vous servir: papille fongiqueL'épithélium invagu est appelé viscéral car il enveloppe les capillaires glomérulaires comme s'ils étaient des viscères. Il est formé par des cellules appelées podocytes qui embrassent, les couvrant, aux capillaires et qui ont des caractéristiques très particulières.
Les podocytes sont organisés en une seule couche, émettant des prolongations qui interdisent avec les extensions des podocytes voisins, laissant des espaces entre eux appelés pores dans des fentes de fente ou de filtration et qui sont des solutions de continuité pour l'étape du filtrage.
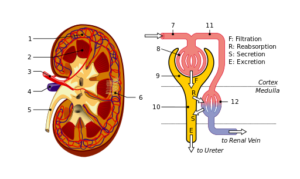 Structure des reins et du néphron: 1. Cortex rénal; 2. Moelle; 3. Artère rénale; 4. Veines rénales; 5. Uretère; 6. Néphrons; 7. Artériola afférente; 8. Glomérule; 9. Capsule Bowman; dix. Tubules et hanle le font; onze. Capillaires péritubulaires (source: fichier: physiologie_of_nephron.SVG: Madhero88File: Kidneysrurtures_piom.SVG: Piotr Michał Jaworski; Piom dans le travail plairivatif: Daniel Sachse (Antares42) [CC BY-SA 3.0 (https: // CreativeCommons.Org / licences / by-sa / 3.0)] via Wikimedia Commons)
Structure des reins et du néphron: 1. Cortex rénal; 2. Moelle; 3. Artère rénale; 4. Veines rénales; 5. Uretère; 6. Néphrons; 7. Artériola afférente; 8. Glomérule; 9. Capsule Bowman; dix. Tubules et hanle le font; onze. Capillaires péritubulaires (source: fichier: physiologie_of_nephron.SVG: Madhero88File: Kidneysrurtures_piom.SVG: Piotr Michał Jaworski; Piom dans le travail plairivatif: Daniel Sachse (Antares42) [CC BY-SA 3.0 (https: // CreativeCommons.Org / licences / by-sa / 3.0)] via Wikimedia Commons) Podocytes et cellules endothéliales qui couvrent une membrane basale sur laquelle elles soutiennent et ont également des solutions de continuité pour le passage de l'eau et des substances. Les cellules endothéliales sont Fenestradas et permettent également la filtration.
Ainsi, ces trois éléments: l'endothélium capillaire, la membrane basale et l'épithélium viscéral de la capsule Bowman, constituent ensemble la membrane ou la barrière de filtration.
Les fonctions
La capsule est associée au processus de filtration glomérulaire. D'une part, car il fait partie de la couverture épithéliale des podocytes qui entoure les capillaires glomérulaires. Il contribue également à la synthèse de la membrane basale sur laquelle cet épithélium et l'endothélium capillaire glomérulaire sont soutenus.
Ces trois structures: l'endothélium capillaire, la membrane basale et l'épithélium viscéral de la capsule Bowman, constituent la barrière de la membrane ou de la filtration, et chacun d'eux a ses propres caractéristiques de perméabilité qui contribuent à la sélectivité globale de cette barrière.
De plus, le volume de liquide qui pénètre dans l'espace Bowman, ainsi que le degré de rigidité que la paroi externe capsulaire s'oppose, détermine la genèse d'une pression intracapsulaire qui aide à moduler la pression de filtration effective et à stimuler le liquide dans tout le tubule associé.
Peut vous servir: périoste: caractéristiques, fonctions et histologieDéterminants de l'ampleur de la filtration glomérulaire
Une variable qui recueille l'ampleur du processus de filtration glomérulaire est le volume de filtration glomérulaire (VFG), qui est le volume de liquide qui est filtré dans tous les glomérules dans l'unité de temps. Sa valeur normale moyenne est d'environ 125 ml / min ou 180 l / jour.
L'ampleur de cette variable est déterminée du point de vue physique par deux facteurs, à savoir le coefficient de filtration ou d'ultrafiltration (KF) SO et la pression de filtration effective (PEFF). C'est-à-dire: vfg = kf x peff (équation 1)
Coefficient de filtration (KF)
Le coefficient de filtration (KF) est le produit de la conductivité hydraulique (LP), qui mesure la perméabilité à l'eau d'une membrane en ML / min par unité de zone et unité de pression de mise en œuvre, par la surface (a) de la membrane filtrante, c'est-à-dire kf = lp x a (équation 2).
L'ampleur du coefficient de filtration indique le volume de liquide filtré par unité de temps et par unité de lecteur efficace. Bien qu'il soit très difficile à mesurer directement, il peut être obtenu à partir de l'équation 1, en divisant VFG / PEFF.
Le KF dans les capillaires glomérulaires est de 12,5 ml / min / mmHg par c / 100 g de tissu, valeur environ 400 fois plus élevé que le KF des autres systèmes capillaires du corps, où vous pouvez filtrer environ 0,01 ml / min / mm Hg par 100 G de tissu. Comparaison montrant l'efficacité du filtrage glomérulaire.
Pression de filtration efficace (PEFF)
La pression de filtration effective représente le résultat de la somme algébrique des différentes forces de pression qui favorisent ou s'opposent à la filtration. Il existe un gradient de pression hydrostatique (ΔP) et une autre pression osmotique (oncotique, Δп) déterminée par la présence de protéines dans le plasma.
Le gradient de pression hydrostatique est la différence de pression entre l'intérieur du capillaire glomérulaire (PCG = 50 mm Hg) et l'espace de capsule Bowman (PCB = 12 mm Hg). Comme on le voit, ce gradient est dirigé du capillaire à la capsule et favorise le déplacement du liquide à cet égard.
Peut vous servir: squelette appendiculaire: fonctions et osLe gradient de pression osmotique déplace le liquide plus petit à une pression osmotique plus élevée. Seules les particules qui ne filtrent pas cet effet. Les protéines ne filtrent pas. Son пCB est 0 et dans le capillaire glomérulaire пCG, il est de 20 mm Hg. Ce gradient déplace le liquide de la capsule vers le capillaire.
La pression effective peut être calculée en appliquant Peff = Δp-Δ; = (PCG-PCB) - (пCG-Oh); = (50-12) - (20-0); = 38-20 = 18 mm Hg. Il existe donc une pression de filtration efficace ou nette d'environ 18 mm Hg qui détermine un VFG d'environ 125 ml / min.
Indice de filtration (IF) des substances présentes dans le plasma
C'est un indicateur de la facilité (ou de la difficulté) avec laquelle une substance présente dans le plasma peut traverser la barrière de filtration. L'indice est obtenu en divisant la concentration de la substance en filtrage (FX) entre sa concentration en plasma (PX), c'est-à-dire: ifx = fx / px.
La plage de valeurs IF se situe entre un maximum de 1 pour les substances qui filtrent librement et 0 pour ceux qui ne filtrent rien. Les valeurs intermédiaires concernent les particules avec des difficultés intermédiaires. Plus la valeur est proche, meilleure est la filtration. Plus près de 0, plus difficile à filtrer.
L'un des facteurs qui détermine la taille de la particule est la taille de la particule. Ceux qui ont des diamètres inférieurs à 4 nm filtre librement (si = 1). À mesure que la taille grandit et s'approche de celle de l'albumine, le Fe est réduit. Les particules de taille d'albumine, ou plus, ont 0 ifs de 0.
Un autre facteur qui aide à déterminer les charges électriques IF est négative sur la surface moléculaire. Les protéines ont beaucoup de charge négative, qui est ajoutée à leur taille pour entraver leur filtrabilité. La raison en est que les pores ont des charges négatives qui repoussent celles des protéines.
Les références
- Ganong WF: fonction rénale et miction, dans Revue de la physiologie médicale, 25e ed. New York, McGraw-Hill Education, 2016.
- Guyton AC, Hall Ji: Le système urinaire, dans Manuel de physiologie médicale , 13e éd, AC Guyton, JE Hall (éd.). Philadelphie, Elsevier Inc., 2016.
- Lang F, Kurtz A: Niere, dans Physiologie des Menschen Pathophysiologie, 31 ed, RF Schmidt et al (eds). Heidelberg, Springer Medizin Verlag, 2010.
- Silbernagl S: Die Funkction Der Nieren, dans Physiologie, 6e Ed; R Klinke et al (eds). Stuttgart, Georg Thieme Verlag, 2010.
- Stahl Rak et al: Niere Undoitende Harnwege, dans Klinche physiopathysiologie, 8th Ed, W Siegenthaler (Ed). Stuttgart, Georg Thieme Verlag, 2001.
- « Que sont les articulations fibreuses? Types et caractéristiques
- Origine de baragonnosie, concept, test, troubles connexes »

