Histoire des cellules HeLa, caractéristiques, cycle cellulaire et utilisations
- 2804
- 501
- Raphaël Meyer
Le Cellules Hela Ils sont un groupe de cellules cancéreuses cultivées en continu depuis 1951, lorsqu'ils ont été isolés d'un patient africain-américain avec une tumeur maligne cervicale. Son nom dérive des deux premières lettres du nom et du nom de famille du patient dont ils ont été obtenus, Henrietta manque (Hela). Ils sont également appelés cellules immortelles, et c'est la plus ancienne lignée cellulaire connue et utilisée par les humains.
La découverte et le développement des cellules HeLa dans la recherche médicale ont été une contribution gigantesque à l'humanité. Ces cellules ont été utilisées dans plus de 70 000 investigations dans le monde.
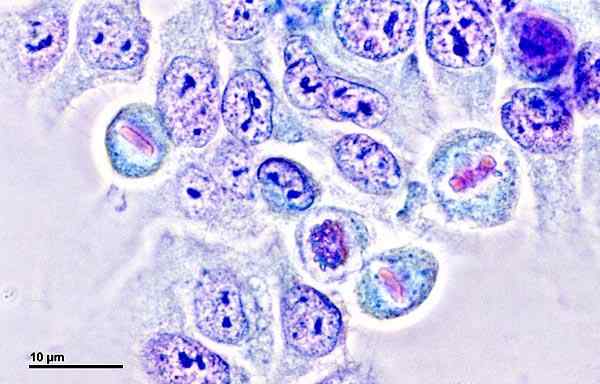
 Culture cellulaire d'Helas. Division des cellules de la métaphase et du profase. Pris et édité à partir de doc. Rnd. Josef Reischig, CSC. [CC BY-SA 3.0 (https: // CreativeCommons.Org / licences / by-sa / 3.0)].
Culture cellulaire d'Helas. Division des cellules de la métaphase et du profase. Pris et édité à partir de doc. Rnd. Josef Reischig, CSC. [CC BY-SA 3.0 (https: // CreativeCommons.Org / licences / by-sa / 3.0)]. Ils étaient un élément fondamental du développement du vaccin contre la polyomyélite et ont été d'une grande aide dans la recherche liée au cancer, au VIH, à la cartographie génétique, entre bien d'autres.
[TOC]
Histoire
Les antécédents des cellules d'Héléa commencent par un patient africain-américain diagnostiqué avec un cancer du col de l'utérus en 1951. Henrietta Lacks est arrivé à l'hôpital Jhon Hopkins, situé dans la ville de Baltimore, dans l'État du Maryland aux États-Unis.
Ce saignement était récurrent après son dernier accouchement et la patiente a également indiqué ressentir une sorte de nœud dans l'utérus. Une analyse du cancer du col de l'utérus a confirmé les soupçons médicaux. Le patient avait une tumeur d'environ 2,5 centimètres de diamètre, facilement palpable.
À ce moment-là, les médecins ont pris le premier échantillon de tissus Henrietta pour une analyse pathologique. Les tests histopathologiques ont indiqué qu'il s'agissait d'un cancer de l'utérus de type spinocellulaire, c'est-à-dire une tumeur maligne avec une prolifération sans contrôle cellulaire.
Le gynécologue traité a mentionné qu'il semblait très atypique qu'après le dernier enfant, la date de diagnostic est une tumeur dans un état de développement aussi avancé.
Avant que le manque Henrietta ne commence son traitement anti-canancer, un résident de l'hôpital avait prélevé un nouveau patient tissu cancéreux et l'avait envoyé au Dr Animal and Human Cell Culture Laboratory. George Otto Gey.
Le patient n'a pas réagi positivement au traitement du cancer, qui consistait en radiation profonde, et huit mois après le diagnostic d'Henrietta a succombé à la maladie à l'âge de 31 ans. Un des médecins traitants a dit qu'il n'avait jamais vu un type de cancer comme ça et ne l'a jamais revu.
Peut vous servir: plasmocytes: caractéristiques, fonctions et maladiesCultures de cellules Hela
Le docteur. George Gey, était un enquêteur éminent des cultures en tissu au Jhon Hopkins Institute. Ce scientifique cherchait une lignée cellulaire immortelle, c'est-à-dire un groupe de cellules qui pouvaient être divisées illimitées dans des conditions de laboratoire (in vitro).
Gey et sa femme ont essayé pendant plus de 20 ans pour obtenir une lignée cellulaire à laquelle ils pouvaient garder indéfiniment dans des conditions de culture. Pour cela, ils s'étaient concentrés sur les cellules cancéreuses, mais ils n'ont pas obtenu les résultats attendus.
C'est alors que le gynécologue et chef du Département de gynécologie de l'Institut Jhon Hopkins, le Dr. Richard Telinde, a recommandé d'utiliser des cellules cervicales, leur fournissant les cellules du patient Henrietta manque.
En soumettant les cellules à Cultvo, ils ont commencé à se multiplier de manière extraordinaire, au rythme d'une génération toutes les 24 heures. Ces résultats ont changé la vie des maris de Gey en tant que chercheurs, ont également changé la médecine et autorisé à innover et à créer de nouveaux domaines de recherche cellulaire.
Pourquoi Henrietta manque?
La découverte des cellules HeLa n'était pas un essai effectué par un seul patient ou donneur. Au contraire, les maris Gey avaient tenté sans succès d'obtenir des cultures cellulaires adéquates de nombreux tissus cancérigènes.
Après la recommandation de Telinde, le couple des chercheurs a convenu d'échantillons de col de l'utérus de divers patients, mais seuls ceux de Henrietta manquent les résultats recherchés.
Une étude menée 20 ans après la mort de Mme. Le manque a révélé que le cancer souffert par ce patient était un type agressif d'adénocarcinome cervical utérin. Par la suite, il a également été appris que les cellules ont été infectées par le papillomavirus humain (HPV).
La souche HPV qui a infecté ces cellules appartient au sérotype 18, qui est précisément associée à des cancers agressifs du col humain.
Les antécédents médicaux du patient ont indiqué, en outre, qu'il souffrait de syphilis. Cela, ainsi que la présence de sérotype HPV 18, pourrait aider à expliquer les résultats obtenus par les maris Gey, en termes de croissance rapide de ces cellules dans des conditions de laboratoire et de leur immortalité.
Caractéristiques
Les cellules Hela sont des cellules cancéreuses. Ils ont une taille de 20 microns de diamètre avec un noyau de 10 microns. Son caryotype et son génome sont inhabituels; D'une part, les gènes sont pleins d'erreurs, et d'autre part, ils ont des copies supplémentaires de certains chromosomes, présentant entre 76 et 80 chromosomes totaux.
Peut vous servir: épithélium plat stratifié: caractéristiques et fonctionIls sont infectés par le papillomavirus humain, la principale cause du cancer du col de l'utérus; Cela fait que certains chromosomes des cellules Helea sont fortement mutés.
Ils ont une croissance considérablement accélérée, même pour être des cellules cancéreuses; De plus, ils sont capables de contaminer et de surmonter une grande variété de cultures cellulaires, de sorte que les précautions doivent être prises lorsque vous travaillez avec eux.
Ce sont des cellules appelées immortelles, car elles peuvent être divisées infiniment dans des conditions idéales. Ils présentent une version active d'une protéine appelée télomérase pendant la division cellulaire.
Cette protéine empêche les cellules thermiques d'atteindre la limite Hayflck. Cette limite a été proposée par Leonard Hayflick et détermine le nombre de fois où une population de cellules normales humaines atteint son niveau de réplication maximum, puis entre en phase de sénescence.
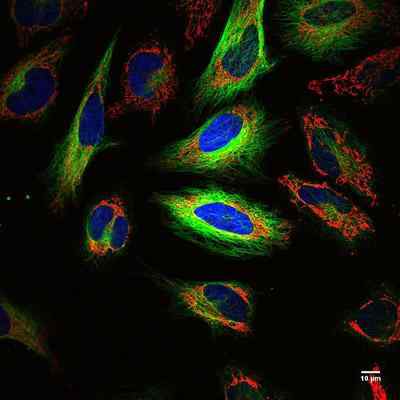 Cellules HeLa, fluorescence multicolore. Pris et édité à partir de 8x57is [cc by-sa 4.0 (https: // CreativeCommons.Org / licences / by-sa / 4.0)].
Cellules HeLa, fluorescence multicolore. Pris et édité à partir de 8x57is [cc by-sa 4.0 (https: // CreativeCommons.Org / licences / by-sa / 4.0)]. Cycle cellulaire
Le cycle cellulaire des cellules Hele n'est pas très différent du cycle cellulaire des autres cellules humaines normales.
Dans les cellules eucaryotes (y compris HeLa), le cycle se compose de 2 phases: une interface, où les cellules se développent et doublent leur matériel génétique et organites, et une phase mitotique, où la cellule sépare son matériel génétique, divise le cytoplasme et donne lieu à un cellule fille.
Les cellules Celus en culture effectuent un cycle de division cellulaire toutes les 20 heures. Dans ce cycle, l'interface est la plus longue étape, avec 19 heures, tandis que la phase mitotique ne dure qu'une heure. Les cellules normales peuvent être divisées en un nombre fini d'occasions tandis que les cellules HeLa peuvent répéter le cycle dans d'innombrables occasions.
Applications
Les chercheurs ont utilisé des cellules HeLa dans plus de 70 000 investigations dans le monde. Leurs utilisations ont été incroyablement variées, certaines d'entre elles ont été des anthiétiques et d'autres ont permis de grandes avancées en médecine.
L'un des cas les plus controversés sur l'utilisation des cellules Helea s'est produit en 1954, lorsqu'un scientifique sans consentement préalable des patients, injecté des cellules HeLa pour évaluer s'ils ont développé un cancer à partir de ces cellules ou non. Ce n'est qu'en 1965 qu'il a été accusé de comportement anthiétique et non professionnel.
Les années après cette affaire ont été très productives pour la médecine et l'histologie. En 1955, Jonas Salks s'est développé et mis à l'aide du vaccin contre la polyomyélite; Il a découvert que les Helas étaient infectés et sont morts par le virus de la polyomyélite, qui a servi à développer un vaccin.
En 1966, la première hybridation des cellules humaines a été réalisée avec celles d'un autre animal (souris) grâce aux cellules Helea.
Peut vous servir: excrétion cellulaireActuellement, les études développées avec les cellules HeLa sont connues qui ont permis d'élargir les connaissances dans des domaines tels que l'immunologie, Avec plusieurs études sur le parvovirus, le virus de l'immunodéficience humaine, la papillomava humaine et la polyomyélite.
En génétique, ils ont été utilisés pour effectuer le séquençage du génome; Ils ont également été utilisés pour comprendre les mécanismes du vieillissement cellulaire, par l'analyse de la reproduction cellulaire et le fonctionnement de l'enzyme télomérase, enzyme impliquée dans un raccourcissement des télomères après chaque division cellulaire.
De plus, les cellules Hela ont aidé à la production de médicaments pour des maladies telles que le mal de Parkinson, la leucémie, entre autres.
Autres utilisations
L'industrie cosmétique les utilise pour s'assurer que les produits n'ont pas d'effets collatéraux indésirables. De plus, ils sont utilisés dans les essais biologiques de tolérance et les effets des substances toxiques sur l'homme.
Les cellules Hela se sont également rendues dans l'espace pendant les missions spatiales des années 70 du siècle dernier. Les scientifiques ont utilisé des cellules HeLa pour connaître les effets de l'absence de gravité sur les cellules humaines.
Les aspects légaux
La plupart des écrits faisant référence aux cellules Hele coïncident dans un aspect général. L'obtention de ces cellules de la patiente Henrietta manque a été faite sans leur consentement et à l'insu de l'utilisation que ces cellules auraient.
Pour les années 50 du siècle dernier, le consentement des patients n'était pas nécessaire pour obtenir des tissus tumoraux. Cependant, aujourd'hui, et grâce en partie à la famille manque, il existe des lois pour protéger le patient.
Ces lois réglementent des aspects tels que la protection des informations médicales des patients, la communication avec les donneurs de cellules, les tissus et la participation aux répétitions ou à la recherche.
 Henrietta manque et son mari. Pris et édité à partir de PROPRE [domaine public].
Henrietta manque et son mari. Pris et édité à partir de PROPRE [domaine public]. Aux États-Unis, il existe des lois étatiques et fédérales qui contrôlent et réglementent le consentement des patients et l'utilisation et l'échange d'informations provenant des dossiers médicaux.
Actuellement pour utiliser les cellules HeLa ou des informations génétiques de ces cellules, il est nécessaire d'être approuvé par un comité. Dans ce comité, entre autres, des parents d'Henrietta manque
Les références
- Hélice. Wikipédia. Récupéré de.Wikipédia.
- Cellules d'Helas. Écarté. Récupéré de Ecured.Cu.
- C. Dosne Pasqualini (2006). HELA Cellules comme prototype de la culture cellulaire immortalisée. Médecine.
- HELA cellules (1951). Société britannique pour l'immunologie. Récupéré de l'immunologie.org.
- Henrietta manque. Encyclopædia Britannica. Britannica a récupéré.com.
- L'héritage d'Henrietta manque. Johns Hopkins Medicine. Récupéré de Hopkinsmedicine.org.
- Phases du cycle cellulaire. Récupéré de es.Khanacademy.org.
- J.P. Álvarez (2013) Henrietta manque. Le nom derrière les cellules Hele, la première ligne immortelle humaine. LOS CONDES MAGAZINE MÉCICIAL CLINIQUE.
- S.M. Portillo (2014).Les cellules Eternal Hela, le dilemme éthique d'aujourd'hui. Magazine médical hondurien.
- « Caractéristiques, structures, fonctions et types de lysosomas
- Caractéristiques de Trichomonas Tenax, morphologie, cycle de vie »

