Caractéristiques, types, fonctions
- 3342
- 956
- Adam Mercier
Le cinases soit kinasesCe sont des protéines à activité enzymatique qui sont responsables du catalyse du transfert de groupes de phosphate (PO4-3) à différents types de molécules. Ce sont des enzymes extrêmement courantes dans la nature, où elles exercent des fonctions transcendantales pour les organismes vivants: le métabolisme participe, la signalisation et aussi dans la communication cellulaire.
Grâce au grand nombre de processus dans lesquels ils remplissent plusieurs fonctions, les kinases sont l'un des types de protéines les plus étudiés, non seulement au niveau biochimique, mais aussi au niveau structurel, génétique et cellulaire.
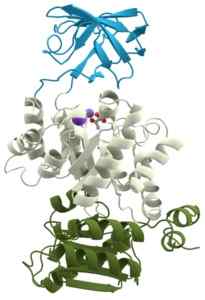
 Domaines de la structure de l'enzyme pyruvato kinase (PYK) Une enzyme glycolytique (Source: Thomas Splettsser (www.Scistyle.com) [cc by-sa 3.0 (https: // CreativeCommons.Org / licences / by-sa / 3.0)] via Wikimedia Commons)
Domaines de la structure de l'enzyme pyruvato kinase (PYK) Une enzyme glycolytique (Source: Thomas Splettsser (www.Scistyle.com) [cc by-sa 3.0 (https: // CreativeCommons.Org / licences / by-sa / 3.0)] via Wikimedia Commons) Il a été déterminé que le génome humain a au moins 500 gènes qui codent pour des enzymes appartenant au groupe de kinases, dont les substrats «accepteurs» de groupes de phosphate peuvent être des glucides, des lipides, des nucléosides, des protéines et d'autres types de molécules organiques.
Ces enzymes sont classées dans le groupe des phosphotransférases (EC 2.7), et utilisent généralement comme molécules «donneurs» phosphate à des composés à haute énergie tels que l'ATP, le GTP, le CTP et d'autres.
[TOC]
Caractéristiques
Le terme «kinase», comme mentionné, se réfère généralement à toutes les enzymes responsables du transfert du groupe de phosphate terminal ATP vers une autre molécule de réception ou «d'acceptation» du groupe phosphate.
Bien que ces enzymes catalysent essentiellement la même réaction de transfert de groupes phosphoryle, il existe une grande diversité parmi celles-ci, non seulement par rapport à la structure, mais à la spécificité des substrats et des voies cellulaires dans lesquelles ils participent.
Généralement, sa structure est composée de feuilles à pelures β et d'hélices α qui sont spécifiquement repliées pour former le site actif, et ledit site actif contient généralement des ions chargés positivement (cations) qui stabilisent les charges négatives des groupes de phosphate qu'ils transfèrent.
Sur l'actif ou à proximité, il existe deux sites de jonction pour les substrats: un pour l'ATP ou la molécule de donateur du groupe phosphate et un autre pour le substrat qui sera phosphorylé.
La réaction générale de ces enzymes (phosphorylation) peut être envisagée comme suit:
Substrat ATP + → ADP + substrat phosphorylé
Où l'ATP fait don du groupe phosphate qui gagne le substrat.
Gars
Selon la classification du comité de nomenclature de l'Union internationale de biochimie et de biologie moléculaire (NC-IBMB), les kinases se trouvent dans le groupe de phosphotransférases (CE. 2.7, enzymes qui transfèrent des groupes qui contiennent du phosphore), qui sont subdivisés, à leur tour, dans environ 14 classes (EC 2.7.1 - EC 2.7.14).
Peut vous servir: hétérose: amélioration des animaux, chez les plantes, l'être humainLes différences fondamentales entre ces 14 types de phosphotransférases sont liées à la nature chimique de la molécule «accepteur» du groupe phosphate qu'ils transfèrent (ou avec la nature de la partie de la molécule que le groupe phosphate reçoit).
Dans cette catégorie (enzymes phosphotransférases), il existe également des enzymes qui transfèrent des phosphates mais n'utilisent pas de molécules d'ATP telles que "donneur", mais utilisent des phosphates inorganiques.
En général, ces classes sont décrites comme suit:
EC 2.7.1: enzymes phosphotransférases qui ont un accepteur de groupe phosphate un alcool
C'est l'un des groupes les plus importants pour le métabolisme énergétique de nombreux organismes, car il contient les enzymes responsables de la phosphorylation des glucides et de leurs dérivés, tels que le glucose, le galactose, le fructose, le mannosa, la glycosamine, le ribose et le ribous, le xylose, le glycérola, la glycosamine, , Pyruvate, Mevalonato, Arabinosa, Inositol, entre autres.
Exemple de ces enzymes communes sont l'hexoquinase, la glycoquinase, la phosphofrucerachinase et la pyruvato kinase, qui sont directement impliquées dans la voie glycolytique qui est responsable de l'oxydation du glucose pour la production d'énergie sous forme d'ATP.
EC 2.7.2: enzymes phosphotransférases qui ont un groupe carboxyle comme accepteur du phosphate
Dans ce type d'enzymes de flinase ou de phosphotransférase se trouvent des enzymes qui transfèrent des groupes de phosphate à des parties de molécules avec des groupes carboxy, tels que l'acétate, le carbamate, l'aspartate, le phosphoglycérate, entre autres.
EC 2.7.3: enzymes phosphotransférases qui ont un atome d'azote comme accepteur du phosphate
Métaboliquement parlant, ce groupe d'enzymes est également d'une grande importance, car ils sont responsables du transfert de groupes de phosphate à des molécules telles que la créatinine, l'arginine, la glutamine, le guanidine-acétate, etc.
EC 2.7.4: enzymes phosphotransférases qui ont un accepteur du groupe phosphate un autre groupe de phosphate
Une grande partie des enzymes de ce groupe travaillent dans la régulation de la formation ou de l'hydrolyse de composés à haute énergie tels que l'ATP, le GTP, le CTP et d'autres, car ils sont responsables de l'addition, de l'élimination ou de l'échange de groupes de phosphate entre ce type de molécules ou ses précurseurs.
Ils participent également au transfert de groupes de phosphate vers d'autres molécules précédemment phosphorylées, qui peuvent être de nature lipidique, de glucides ou dérivées de celles-ci.
Exemple de ces enzymes importantes sont l'adénylate de kinase, la phosphate kinase nucléoside, la kinase de l'adénylate de tryposphate nucléoside, la kinase UMP / CMP et la phosphate kinase Farnesil, etc.
EC 2.7.6: enzymes diposfotransférases
Les diposfotransférases catalysent le transfert de deux groupes de phosphate simultanément vers le même substrat. Exemple de ces enzymes sont la diffosphoquinase ribose-phosphate, la diffosphoquinase thiamine et le GTP de la défosphoquinase, qui est une enzyme importante dans le métabolisme des purines.
Peut vous servir: sphingomyline: qu'est-ce que la structure, les fonctions, la synthèseEC 2.7.7: enzymes spécifiques de nucléotide phosphotransféransférase (nucléotides phosphotransférases)
Les nucléidos phosphotransférases participent à de nombreux processus cellulaires impliqués dans l'activation et l'inactivation d'autres protéines et enzymes, ainsi que dans certains mécanismes de réparation de l'ADN.
Sa fonction consiste à transférer des nucléotides, généralement des nucléotides monophosphates de différentes bases d'azote. Dans ce type d'enzymes se trouvent l'ADN et l'ARN polymérases (ADN et ARN dépendant), l'Uridiltransférase UDP-glucosa 1-phosphate uridiltransférase, entre autres.
EC 2.7.8: enzymes qui transfèrent des groupes de phosphate par des substitutions
Cette classe a des fonctions significatives dans les voies de métabolisme des lipides, en particulier dans sa synthèse. Ils sont responsables du transfert de molécules phosphorylées (phosphates par substitutions) vers d'autres molécules "accepteur".
Un exemple de ce groupe d'enzymes est la phosphotransférase éthanolamine, la diacylglycérol colina phosphotransférase, la sphingomyeline synthase, etc.
EC 2.7.9: enzymes phosphotransférases avec accepteurs appariés
Ces enzymes utilisent un seul donneur de groupe phosphate (ATP ou lié) pour phosphoryler deux molécules d'accepteur différentes. Le pyruvate de phosphate déchaîné (PPDK) et la phosphoglucano dicinase sont des exemples de ces enzymes.
Phosphotransférases qui phosphorylent les résidus d'acides aminés de différents types de protéines
EC 2.7.10: protéine-lyrosine kinases
Les protéines-pyrosine kinases sont des enzymes qui catalysent le transfert de groupes de phosphate spécifiquement dans les résidus de tyrosine dans les chaînes polypeptidiques de différents types d'accepteurs de protéines.
EC 2.7.11: Kinases protéine-sérine / treonine
Comme le font les protéines-pyrosine kinases, ce groupe d'enzymes catalyse le transfert de groupes de phosphate à la sérine ou aux déchets de tréonine dans d'autres protéines.
Un exemple connu de ces protéines est la famille des protéines kinases C, qui participent à plusieurs manières, mais surtout au métabolisme lipidique.
Ce groupe comprend également de nombreuses protéines cycliques dépendantes de l'AMP et GMP cyclique, avec des implications importantes dans la différenciation cellulaire, la croissance et la communication.
EC 2.7.12: Les kinases sont une double spécificité (qui peut agir à la fois en sérine / treonine et en déchets de tyrosine)
Les protéines des kinases activées par les mitogènes (MAPKK) font partie de ce groupe d'enzymes capables de seine, de tréonine ou de tyrosine du déchet d'autres protéines kinases.
Histidin Mutkish (EC 2.7.13) et les kinases protéine-arginine (EC 2.7.14)
Il existe d'autres protéines kinases capables de transférer des groupes de phosphate vers l'histidine et les résidus d'arginine dans certains types de protéines et ce sont des protéines kinases et des kinases protéine-arginine.
Autres formes de classification
Selon différents auteurs, les kinases peuvent être mieux classées en fonction du type de substrat qu'ils utilisent comme accepteur de groupe phosphate.
Peut vous servir: nucléoside: caractéristiques, structure et applicationsD'autres considèrent que la meilleure façon de classer ces enzymes est en fonction de la structure et des caractéristiques de leur site actif, c'est-à-dire, selon la conformation et la présence d'ions ou de certaines molécules dans le même.
Selon le type de substrat, les kinases peuvent être classées comme protéine de la cinase (qui phosphorylent d'autres protéines), les lipa kinases (qui phosphorylent les lipides), les glucides kinases (qui phosphorylent différents types de glucides), les nucléosides phosphoryles (qui phosphoryllal nucléosides), etc.
Les fonctions
Les enzymes du groupe kinase sont de nature omniprésente et une seule cellule peut abriter des centaines de types différents, catalysant les réactions sur plusieurs routes cellulaires.
Ses fonctions peuvent être très diverses:
-Ils participent à plusieurs processus de signalisation et de communication cellulaire, en particulier les protéines kinases, qui catalysent la phosphorylation consécutive d'autres protéines kinases (cascades de phosphorylation) en réponse aux stimuli internes et externes.
-Certaines de ces protéines à activité enzymatique ont des fonctions centrales dans le métabolisme des glucides, les lipides, les nucléotides, les vitamines, les cofacteurs et les acides aminés. Par exemple, rien de plus dans la glycolyse participe à au moins 4 kinases: l'hexochinase, la phosphofrucerachinase, la phosphoglycérate kinase et la pyruvate kinase.
-Parmi les fonctions de signalisation, les kinases sont impliquées dans les processus de régulation de l'expression génétique, de la contraction musculaire et de la résistance aux antibiotiques dans différents types d'organismes vivants.
-Les protéines de putter-chinase ont des fonctions dans la régulation de nombreuses voies de transduction du signal qui sont liées au développement et à la communication dans les métazos multicellulaires.
-La modification des protéines de phosphorylation (dans d'autres contextes cellulaires autres que la signalisation cellulaire) est un élément important de régulation de l'activité de grandes quantités d'enzymes qui participent à différents processus métaboliques. Tel est l'exemple de la régulation du cycle cellulaire par de nombreuses protéines dépendantes de la kinase.
-Les kinases phosphoriillaires lipidiques sont essentielles pour les processus de remodelage des membranes cellulaires, ainsi que la synthèse et la formation de nouvelles membranes.
Les références
- Joues., Zhang, H., & Grishin, n. V. (2002). Séquence et classification de la structure des kinases. Journal of Molecular Biology, 2836(02), 855-881.
- Cooper, J. (2018). Britannica Encyclopaedia. Récupéré de Britannica.com
- Da silva, g. (2012). Progrès des protéines kinases. Rijaka, Croatie: Intech Open.
- Krebs, E. (1983). Perspectives historiques sur la phosphorylation des protéines et un système de classification pour les protéines kinases. Phil. Trans. R. Soc. Lond. B, 302, 3-11.
- Krebs, E. (1985). La phosphorylation des protéines: un mécanisme majeur de régulation biologique. Transactions de la société biochimique, 13, 813-820.
- Comité de nomenclature de l'Union internationale de biochimie et de biologie moléculaire (NC-IBMB). (2019). Récupéré de qmul.CA.ROYAUME-UNI
- « Caractéristiques du glutathion, structure, fonctions, biosynthèse
- Caractéristiques de mouvement rectiligne uniforme, formules, exercices »

