Chaleur de réaction
- 4184
- 662
- Paul Dumas
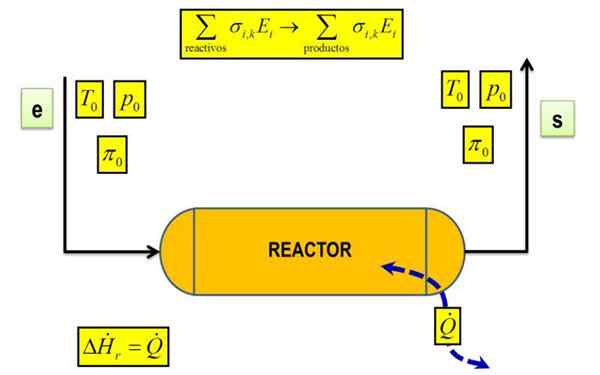
 Schéma de chaleur de réaction dans certaines conditions de température et de pression. Source: JoseaSorrentino, CC BY-SA 4.0, Wikimedia Commons
Schéma de chaleur de réaction dans certaines conditions de température et de pression. Source: JoseaSorrentino, CC BY-SA 4.0, Wikimedia Commons Qu'est-ce que la chaleur de réaction?
Il chaleur de réaction, o L'enthalpie de réaction (ΔH), est la quantité d'énergie par mole qui est libérée ou produite dans une réaction chimique à une pression constante. Il s'agit d'une unité thermodynamique de mesure utile pour calculer l'énergie libérée ou produite.
Puisque l'enthalpie dérive de la pression, du volume et de l'énergie interne, qui sont toutes des fonctions d'état, l'enthalpie est également une fonction d'état.
ΔH, ou le changement d'enthalpie, est apparu comme une unité de mesure visant à calculer le changement d'énergie d'un système lorsqu'il est devenu trop difficile de trouver ΔU, ou un changement dans l'énergie interne d'un système, mesurant simultanément la quantité de chaleur et travail échangé.
Donner.
La notation ΔHº ou ΔHºr puis se pose pour expliquer la température et la pression précises de la chaleur de réaction ΔH.
L'enthalpie de réaction standard est symbolisée par ΔHº ou ΔHºrxn et peut supposer des valeurs à la fois positives et négatives. Les unités pour ΔHº sont des kilojuos par mol, ou kj / mol.
Concept antérieur pour comprendre la chaleur de réaction: différences entre ΔH et ΔHºr
- Δ = représente le changement d'enthalpie (enthalpie des produits sauf l'enthalpie des réactifs).
Une valeur positive indique que les produits ont une plus grande enthalpie, ou qu'il s'agit d'une réaction endothermique (la chaleur est nécessaire).
Une valeur négative indique que les réactifs ont une plus grande enthalpie, ou qu'il s'agit d'une réaction exothermique (la chaleur se produit).
- º = signifie que la réaction est un changement d'enthalpie standard et se produit à une pression / température pré-établi.
- R = indique que ce changement est l'enthalpie de la réaction.
Peut vous servir: Calcium: propriétés, structure, obtenir, utiliser- L'état standard: l'état standard d'un solide ou d'un liquide est la substance pure à une pression de 1 bar, ou ce qui est le même, 1 atmosphère (105 pa) et une température de 25 ° C, ou ce qui est le même, 298 k.
- Le ΔHºr C'est la chaleur standard de réaction ou l'enthalpie standard d'une réaction, et comme ΔH mesure également l'enthalpie d'une réaction. Cependant, ΔHºrxn se déroule dans des conditions «standard», ce qui signifie que la réaction a lieu à 25 ° C et 1 atm.
L'avantage d'une mesure ΔH dans des conditions standard réside dans la capacité de relier une valeur de ΔHº avec une autre, car elles se produisent dans les mêmes conditions.
Chaleur de formation
La chaleur de formation standard, ΔHFº, d'un produit chimique est la quantité de chaleur absorbée ou libérée de la formation de 1 mol de ce produit chimique à 25 ° C et 1 bar de ses éléments dans ses états standard.
Un élément est dans son état standard s'il est dans sa forme la plus stable et sa condition physique (solide, liquide ou gaz) à 25 ° C et 1 bar.
Par exemple, la chaleur standard de formation du dioxyde de carbone implique l'oxygène et le carbone comme réactifs.
L'oxygène est plus stable comme des molécules de gaz ou2, Alors que le carbone est plus stable comme le graphite solide (le graphite est plus stable que le diamant dans des conditions standard).
Pour exprimer la définition d'une autre manière, la chaleur standard de formation est un type spécial de chaleur de réaction standard.
La réaction est la formation de 1 mole d'un produit chimique de ses éléments dans ses états standard dans des conditions standard.
Peut vous servir: caractère métalliqueLa chaleur standard de la formation est également appelée enthalpie standard de la formation (bien que ce soit vraiment un changement d'enthalpie).
Par définition, la formation d'un élément de lui-même ne produirait aucun changement d'enthalpie, de sorte que la chaleur de réaction standard pour tous les éléments est nul.
Calcul de l'enthalpie de réaction
1. Calcul expérimental
L'enthalpie peut être mesurée expérimentalement en utilisant un calorimètre. Un calorimètre est un instrument où un échantillon est réagi à travers des câbles électriques qui fournissent une énergie d'activation. L'échantillon se trouve dans un récipient entouré d'eau, qui est constamment agité.
Lorsqu'il est en mesure avec un calorimètre, le changement de température qui se produit lorsque l'échantillon réagit, et la connaissance de la chaleur spécifique de l'eau et de sa masse, la chaleur qui libère ou absorbe la réaction est calculée par l'équation Q = CESP X M X ΔT.
Dans cette équation, quelle est la chaleur, CESP est la chaleur spécifique, dans ce cas d'eau, qui est égale à 1 calorique par gramme, M est la masse d'eau et ΔT est le changement de température.
Le calorimètre est un système isolé qui a une pression constante, donc ΔHr= q
2. Calcul théorique
Le changement d'enthalpie ne dépend pas de la voie particulière d'une réaction, mais uniquement du niveau d'énergie mondiale des produits et réactifs. Entalpía est fonction de l'État, et en tant que tel, il est additif.
Pour calculer l'enthalpie standard d'une réaction, nous pouvons ajouter les enthalpies standard de la formation de réactifs et la soustraire de la somme des enthalpies de formation de produits standard. Mathématiquement, cela nous donne:
Il peut vous servir: 6 indicateurs de pH naturels et leurs caractéristiquesΔHr° = σ ΔHFº (produits) - σ ΔHFº (réactifs).
Les enthalpies réactions sont généralement calculées à partir des enthalpies de formation de réactifs dans des conditions normales (pression et température de 1 bar 25 ° C).
Pour expliquer ce principe de thermodynamique, nous calculerons l'enthalpie de la réaction pour la combustion du méthane (CH4) Selon la formule:
Ch4 (g) + 2e2 (g) → Co₂ (g) + 2H2O (g)
Pour calculer l'enthalpie de réaction standard, nous devons rechercher des enthalpies de formation standard pour chacun des réactifs et produits impliqués dans la réaction.
Ceux-ci se trouvent normalement dans une annexe ou dans plusieurs tables en ligne. Pour cette réaction, les données dont nous avons besoin sont:
HFCh4 (g) = -75 kjour / mol.
HFº O2 (g) = 0 kjour / mol.
HFº Co₂ (g) = -394 k roul / mol.
HFº h₂o (g) = -284 kjour / mol.
Notez que parce qu'il est dans son état standard, l'enthalpie standard de formation de gaz est 0 kJ / mol.
Ensuite, nous résumons nos enthalpies de formation standard. Gardez à l'esprit que parce que les unités sont en KJ / Mol, nous devons nous multiplier par les coefficients stoechiométriques dans l'équation de réaction équilibrée.
Σ ΔHFº (produits) = ΔHFº Co₂ +2 ΔHFº H₂o
Σ ΔHFº (produits) = -1 (394 koul / mol) -2 (284 koul / mol) = -962 kjour / mol
Σ ΔHFº (réactifs) = ΔHFCh4 + ΔHFº O2
Σ ΔHFº (réactifs) = -75 Koul / mol + 2 (0 kjour / mol) = -75 kjour / mol
Maintenant, nous pouvons trouver l'enthalpie standard de la réaction:
ΔHr° = σ ΔHFº (produits) - σ ΔHFº (réactifs) = (- 962) - (- 75) =
ΔHr° = - 887kj / mol.
Les références
- Enthalpie de définition de la réaction. Récupéré de Thoughtco.com.
- (S.F.). Enthalpie standard de réaction. Récupéré de Boundless.com.

