Alcools
- 3296
- 411
- Prof Noah Collet
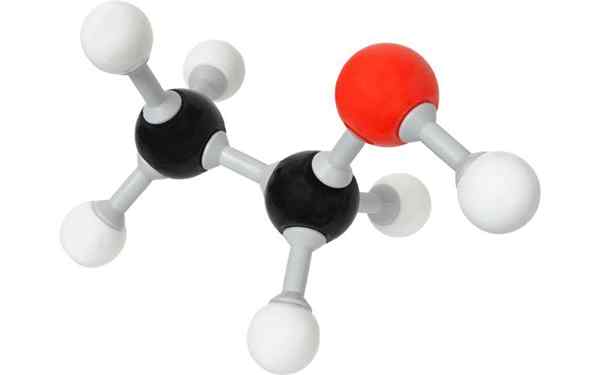
 Molécule d'éthanol ou alcool éthylique. Avec licence
Molécule d'éthanol ou alcool éthylique. Avec licence Que sont les alcools?
Les Alcools Ce sont des composés organiques caractérisés par un groupe hydroxyle (-OH) lié à un carbone saturé, c'est-à-dire un carbone lié à quatre atomes par des liaisons simples (sans liens doubles ou triples).
La formule générique pour cette vaste et polyvalente famille de composés est Roh. Pour être considéré comme de l'alcool dans un sens strictement chimique, le groupe OH doit être le plus réactif de la structure moléculaire. Ceci est important pour affirmer, parmi plusieurs molécules avec des groupes OH, qui sont un alcool.
L'un des alcools par excellence et le plus connu dans la culture populaire est l'alcool éthylique, ou l'éthanol, CH3Ch2Oh. Selon leur origine naturelle, et donc de leur environnement chimique, leurs mélanges peuvent provoquer un spectre illimité de saveurs, certains, qui montrent même des changements positifs au palais au cours des années.
Structure des alcools
Les alcools ont une formule générale ROH. Le groupe OH est lié au groupe r alquilical, dont la structure varie d'un alcool à un autre. Le syndicat entre R et OH est un simple lien covalent, R-oh.
L'image suivante montre trois structures génériques pour les alcools, étant donné que l'atome de carbone est saturé, c'est-à-dire qu'il forme quatre liens simples.
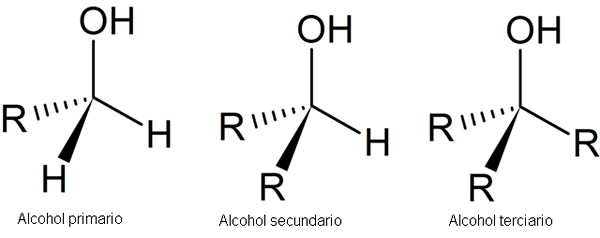 Structure des alcools. Source: Secalinum, Wikimedia Commons
Structure des alcools. Source: Secalinum, Wikimedia Commons Comme on peut le voir, R peut être n'importe quelle structure gazéifiée tant qu'elle ne possède pas plus de substituants réactifs que le groupe OH.
Dans le cas de l'alcool primaire, le 1er, le groupe OH est lié à un carbone primaire. Ceci est facilement vérifié en observant que l'atome au centre du tétraèdre gauche est lié à un R et deux H.
L'alcool secondaire, 2e, est vérifié avec le carbone du tétraèdre du centre maintenant lié à deux groupes R et à un H.
Et enfin, vous avez de l'alcool tertiaire, 3e, avec du carbone lié à trois groupes R.
Caractère amphifile
Selon le type de carbone lié à OH, vous avez la classification des alcools primaires, secondaires et tertiaires. Dans le tétraèdre, les différences structurelles entre elles étaient déjà détaillées. Mais tous les alcools, quelle que soit leur structure, partagent quelque chose en commun: le personnage des amphiphiles.
Il n'est pas nécessaire de traiter une structure pour le remarquer, mais cela suffit avec sa formule chimique ROH. Le groupe de location est presque entièrement constitué.
D'un autre côté, le groupe OH peut former des ponts d'hydrogène avec les molécules d'eau, ce qui est donc hydrophyle, c'est-à-dire qu'il présente une affinité pour l'eau. Ensuite, les alcools ont un squelette hydrophobe, avec un groupe hydrophile. Ils sont apolaires et polaires en même temps, ce qui est le même que de dire qu'ils sont des substances amphifiles.
Peut vous servir: différences entre les mélanges homogènes et les mélanges hétérogènesR-OH
(Hydrophobe) - (hydrophile)
Comme cela sera expliqué dans la section suivante, le caractère amphifile des alcools définit certaines de leurs propriétés chimiques.
Structure de r
Le groupe de location peut avoir n'importe quelle structure, et pourtant il est important car il permet aux alcools d'être classés.
Par exemple, R peut être une chaîne ouverte, comme c'est le cas avec l'éthanol ou le propanol, ramifiée, comme l'alcool T-butyle (CH3)2Chch2Oh, il peut être cyclique, comme dans le cas du cyclohexanol, ou peut avoir une bague aromatique, comme dans l'alcool benzylique (C6H5) Ch2Oh, ou en 3-Fenilpropanol (C6H5) Ch2Ch2Ch2Oh.
La chaîne R peut même avoir des substituants tels que les halogènes ou les doubles liais3Ch2= Chch2OH).
Compte tenu de la structure de R, la classification des alcools devient complexe. Par conséquent, la classification basée sur sa structure (1er, 2e et 3e alcools) est plus facile mais moins spécifique, bien qu'elle soit suffisante pour expliquer la réactivité des alcools.
Proprietes physiques et chimiques
- Point d'ébullition: L'une des principales propriétés des alcools est qu'ils sont associés à des ponts d'hydrogène. Grâce à cela, les alcools sont généralement liquides avec des points d'ébullition élevés.
- Capacité de solvant: Dans les maisons, il est très courant de recourir à l'utilisation d'alcool isopropylique pour éliminer une tache difficile à éliminer sur une surface. Cette capacité de solvant, très utile pour la synthèse chimique, est due à son caractère amphropifil, expliqué précédemment. Les graisses sont caractérisées par une hydrophobe: c'est pourquoi il est difficile de les retirer avec de l'eau. Cependant, contrairement à l'eau, les alcools ont une partie hydrophobe de leur structure. Ainsi, sa location de groupe interagit avec les graisses, tandis que le groupe OH forme des ponts d'hydrogène avec de l'eau, aidant à les déplacer.
- Anfotérisme: Les alcools peuvent réagir sous forme d'acides et de bases, c'est-à-dire ce sont des substances amphotentes. Ceci est représenté avec les deux équations chimiques suivantes:
Roh + h+ => Roh2+
Roh + oh- => Ro-
Le ro- C'est la formule générale de ce qui est connu comme un alcoxyde.
Nomenclature
Il existe deux façons de nommer des alcools, dont la complexité dépendra de leur structure.
Nom comun
Les alcools peuvent être appelés à leurs noms communs. Pour ce faire, le nom du groupe R doit être connu, à laquelle la fin -ico est ajoutée, et est précédée par le mot «alcool». Par exemple, Cho3Ch2Ch2Oh est l'alcool propylico.
Peut vous servir: système hétérogèneLes autres exemples sont:
- Ch3OH: alcool méthylique.
- (Ch3)2Chch2OH: alcool isobutyl.
- (Ch3)3COH: alcool tert-bultyle.
Système IUPAC
Quant aux noms communs, vous devez commencer par identifier r. L'avantage de ce système est qu'il est beaucoup plus précis que l'autre.
A, comme c'est un squelette de carbone, il peut avoir des ramifications ou plusieurs chaînes. La chaîne la plus longue, c'est-à-dire avec plus d'atomes de carbone, est auquel le nom de l'alcool sera décerné.
Le nom de la chaîne la plus longue est ajouté au nom de l'alcane, la terminaison «l» est ajoutée. C'est pourquoi Cho3Ch2Oh s'appelle l'éthanol (Cho3Ch2- + OH).
Généralement, oh doit avoir le moins d'énumération possible. Par exemple, le brch2Ch2Ch2(Oh) Cho3 Il s'appelle le 4-bromo-2-butanol, et non le 1-bromo-3-butanol.
La synthèse
Hydratation des alcènes
Le processus de lait d'huile produit un mélange de quatre ou cinq atomes de carbone, qui peuvent facilement se séparer.
Ces alcènes peuvent devenir des alcools par l'ajout direct de l'eau ou par la réaction de l'alcène avec de l'acide sulfurique, suivi de l'ajout de l'eau que l'acide divise, originaire de l'alcool.
Procédé oxo
En présence d'un catalyseur adéquat, les alcènes réagissent avec le carbone et le monoxyde d'hydrogène pour générer des aldéhydes. Les aldéhydos peuvent être facilement réduits à des alcools par une réaction d'hydrogénation catalytique.
Il y a souvent une telle synchronisation du processus oxo que la réduction des aldéhydos est presque simultanée avec leur formation.
Le catalyseur le plus utilisé est le décobalto octocarbonil, obtenu par la réaction entre le cobalt et le monoxyde de carbone.
Fermentation des glucides
La fermentation des glucides pour la levure est encore d'une grande importance dans la production d'éthanol et d'autres alcools. Les sucres proviennent de canne à sucre ou d'amidon obtenu à partir de différents grains. Pour cette raison, l'éthanol est également appelé "alcool de céréales"
Applications
Boisson
- Bien que ce ne soit pas la fonction principale des alcools, la présence d'éthanol dans certaines boissons est l'une des connaissances les plus populaires. Ainsi, l'éthanol, le produit de la fermentation de la canne à sucre, des raisins, de la pomme, etc., Il est présent dans de nombreuses boissons à la consommation sociale.
Matière première chimique
- Le méthanol est utilisé dans la production de formaldéhyde, par son oxydation catalytique. Le formaldéhyde est utilisé dans la fabrication de plastiques, de peintures, de textiles, d'explosifs, etc.
- Le butanol est utilisé dans la production de butanoat butane, un ester utilisé comme arôme dans l'industrie alimentaire et la confiserie.
- L'alcool allyique est utilisé dans la production d'esters, y compris le phtalate de Dialilo et l'isftalate de Dialilo, qui servent de monomères.
- Le phénol est utilisé dans la production de résines, la fabrication en nylon, les déodorants, les cosmétiques, etc.
- Les alcools de chaîne linéaire de 11 à 16 atomes de carbone sont utilisés comme intermédiaires pour obtenir des plastifiants. Par exemple, le chlorure de polyvinyle.
- Les alcools gras so-appelés sont utilisés comme intermédiaires dans la synthèse des détergents.
Solvants
- Le méthanol est utilisé comme solvant de peinture, ainsi que le 1-butanol et l'alcool isobutilique.
- L'alcool éthylique est utilisé comme solvant de nombreux composés insolubles dans l'eau, en utilisant comme solvant dans les peintures, les cosmétiques, etc.
- Les alcools gras sont utilisés comme solvants dans l'industrie textile, dans les colorants, dans les détergents et dans les peintures. L'isobutanol est utilisé comme solvant dans le matériel de revêtement, les peintures et les adhésifs.
Carburant
- Le méthanol est utilisé comme carburant dans les moteurs à essence internes et additifs pour améliorer la combustion.
- L'alcool éthylique est utilisé en combinaison avec des combustibles fossiles dans les véhicules à moteur. À cette fin, de vastes régions du Brésil sont destinées à la culture de la canne à sucre pour la production d'alcool éthylique. Cet alcool a l'avantage de produire dans sa combustion uniquement de dioxyde de carbone. Lorsque l'alcool éthylique est brûlé, il produit une flamme propre et sans fumée, c'est pourquoi il est utilisé comme carburant dans les cuisines de campagne.
- L'alcool gélifié est produit par combinaison de méthanol ou d'éthanol avec de l'acétate de calcium. Cet alcool est utilisé comme source de chaleur dans les poêles à la campagne, et comme il se répand, il est plus sûr que les alcools liquides.
- Le biobutanol so-appelé est utilisé comme carburant de transport, ainsi que l'alcool isopropylique, bien que son utilisation ne soit pas recommandée.
Antiseptiques
- 70% de concentration L'alcool isopropylique est utilisé comme antiseptique externe pour l'élimination des germes et le retard de sa croissance, tout comme l'alcool éthylique.
Autres utilisations
- Le cyclohexanol et le méthylciclohexanol sont utilisés dans la finition textile, les meubles transformés et les chitamanchas.
Exemples d'alcools et de leurs formules
- Méthanol (ch3OH).
- 1-propanol (c3H7OH).
- Éthanol (c2H5OH).
- Isobutanol (c4H9OH).
- Isopropanol (c3H8SOIT).
- Alcool allique (C3H6SOIT).
- Alcool benzylique (c7H8SOIT).
- Thermique (c₄h₁₀o).
- Pentenol (C5HonzeOH).
- 2-butanol (ch3-Ch2-Choh-ch3).
- Phénol (c6H6SOIT).
- 2-propanol (ch3-Choh-ch3).
- Isodecanol (c10H21OH).
- Alcool cétyl (c16H3. 4SOIT).
- Alcool propargilique (C3H4SOIT).
- Alcool tétrahydrofurilique (C5H10SOIT2).
- Cyclohexanol (c6H12SOIT).
- 2-chlorotanol (c2H5Clo).
- Heptanol (c7H16SOIT).
- Hexanol (c₆h₁₄o).
Les références
- Chimie organique. Mc Graw Hill.
- Alcools. Récupéré de Colapret.cm.Utexas.Édu.

