Concept d'agent oxydant, les exemples les plus forts
- 4782
- 1439
- Mlle Ambre Dumont
UN agent d'oxydation C'est un produit chimique qui a la capacité de soustraire des électrons d'une autre substance (agent réducteur) qui les donne ou les perd. Il est également connu comme un agent oxydant à cet élément ou composé qui traverse les atomes électronégatifs à une autre substance.
Lorsque les réactions chimiques sont étudiées, toutes les substances impliquées et les processus qui se produisent dans ceux-ci doivent être pris en compte. Parmi les plus importants figurent les réactions de réduction de l'oxyde, également appelées redox, qui impliquent le transfert ou le transfert d'électrons entre deux ou plusieurs espèces chimiques.

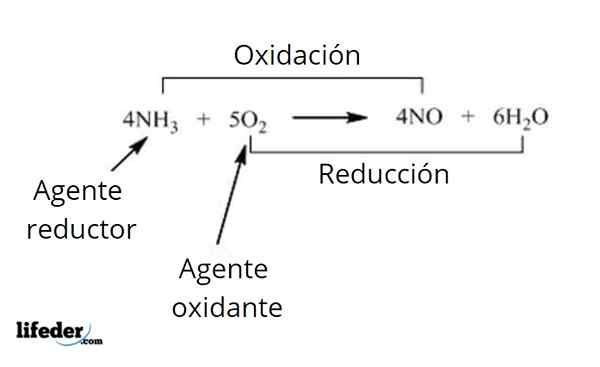
Dans ces réactions, deux substances interagissent: l'agent réducteur et l'agent oxydant. Certains des agents oxydants qui peuvent être observés plus fréquemment sont l'oxygène, l'hydrogène, l'ozone, le nitrate de potassium, le perborate de sodium, les peroxydes, les halogènes et les composés du permananate, entre autres.
L'oxygène est considéré comme le plus courant des agents oxydants. À titre d'exemple de ces réactions organiques qui impliquent le transfert d'atomes, la combustion se démarque, qui consiste en une réaction produite entre l'oxygène et un autre matériau oxyable.
[TOC]
Que sont les agents oxydants?
En semi-repaction d'oxydation, l'agent oxydant est réduit car, lors de la réception d'électrons de l'agent réducteur, une diminution de la valeur de la charge ou du nombre d'oxydation de l'un des atomes de l'agent oxydant est induit.
Cela peut s'expliquer par l'équation suivante:
2 mg (s) + o2(g) → 2mgo (s)
It can be seen that magnesium (mg) reacts with oxygen (O2), and that oxygen is the oxidizing agent because it subtracts electrons from magnesium - that is, it is being reduced - and magnesium becomes, in turn, in turn, In the agent de réaction de réaction.
Il peut vous servir: calcogens ou amphumosDe même, la réaction entre un fort agent oxydant et un agent réducteur fort peut être très dangereux car ils peuvent interagir violemment, ils doivent donc être stockés dans des sites séparés.
Quels facteurs définissent la force d'un agent oxydant?
Ces espèces se distinguent en fonction de leur "force". C'est-à-dire que les plus faibles sont ceux qui ont une capacité inférieure à soustraire les électrons d'autres substances,.
Au lieu de cela, les plus forts ont une plus grande facilité ou capacité à "démarrer" ces électrons. Pour leur différenciation, les propriétés suivantes sont prises en compte:
Radio atomique
Il est connu comme la moitié de la distance qui sépare les noyaux de deux atomes d'éléments métalliques adjacents ou de "voisins".
Les radios atomiques sont généralement déterminées par la force avec laquelle les électrons les plus superficiels sont attirés par le noyau atome.
Par conséquent, le rayon atomique d'un élément diminue dans le tableau périodique de bas en haut et de gauche à droite. Cela implique que, par exemple, le lithium a un rayon atomique significativement plus grand que le fluorure.
Électronégativité
L'électronégativité est définie comme la capacité d'un atome à capturer des électrons appartenant à une liaison chimique à lui-même. À mesure que l'électronégativité augmente, les éléments ont une tendance croissante pour attirer les électrons.
En termes généraux, l'électronégativité augmente de gauche à droite dans le tableau périodique et diminue tandis que le caractère métallique se développe, le fluor étant l'élément le plus électronégatif.
Affinité électronique
On dit que c'est la variation de l'énergie qui est enregistrée lorsqu'un atome reçoit un électron pour générer un anion; C'est-à-dire que c'est la capacité d'une substance à recevoir un ou plusieurs électrons.
Peut vous servir: substitution électrophile aromatique: mécanisme et exemplesÀ mesure que l'affinité électronique augmente, la capacité oxydative d'une espèce chimique augmente.
Énergie d'ionisation
C'est la quantité minimale d'énergie nécessaire pour démarrer un électron à partir d'un atome ou, en d'autres termes, est une mesure de la "force" avec laquelle un électron est lié à un atome.
Plus la valeur de cette énergie est grande, le détachement d'un électron est plus difficile. Ainsi, l'énergie d'ionisation est élargie de la gauche de la droite et est réduite de haut en bas dans le tableau périodique. Dans ce cas, les gaz nobles ont de grandes valeurs d'énergie d'ionisation.
Les agents oxydants les plus forts
En tenant compte de ces paramètres des éléments chimiques, il est possible de déterminer quelles sont les caractéristiques que les meilleurs agents oxydants doivent avoir: une électronégativité élevée, sous la radio atomique et une énergie à haute ionisation.
Cela dit, les meilleurs agents oxydants sont pris en compte qui sont capables d'oxyder un grand nombre de substances.
Exemples de réactions avec les agents oxydants
Dans certaines réactions de réduction de l'oxyde, il est plus facile de visualiser le transfert d'électrons que dans les autres. Certains des exemples les plus représentatifs seront expliqués ci-dessous:
Exemple 1
La réaction de décomposition de l'oxyde de mercure:
2hgo (s) → 2Hg (l) + o2(g)
Dans cette réaction, le mercure (agent oxydant) se distingue comme le récepteur d'électrons d'oxygène (agent réducteur), en décomposition du mercure liquide et de l'oxygène du gaz lors du chauffage.
Il peut vous servir: acide láurique: structure, propriétés, utilisations, avantages, effetsExemple 2
Une autre réaction qui illustre l'oxydation est celle de la combustion de soufre en présence d'oxygène pour former du dioxyde de soufre:
S (s) + o2(g) → Donc2(g)
Ici, on peut voir que la molécule d'oxygène est oxydée (agent réducteur), tandis que le soufre élémentaire est réduit (agent oxydant).
Exemple 3
Enfin, la réaction de combustion au propane (utilisée dans le gaz pour le chauffage et la cuisine):
C3H8(g) + 5o2(g) → 3CO2(g) + 2h2Ou (l)
Dans cette formule, la réduction de l'oxygène (agent oxydant) peut être observée.
Les références
- Agent réducteur. Récupéré de.Wikipédia.org
- Chang, R. (2007). Chemistry, neuvième édition (McGraw-Hill).
- Malone, L. J., Et Dolter, t. (2008). Concepts de base de la chimie. Récupéré des livres.Google.co.aller
- Reflue, D., Et gammon, s. D. (2010). Chimie générale, édition améliorée. Récupéré des livres.Google.co.aller
- Kotz, J., Treichel, P., Et Towsend, J. (2009). Chimie et réactivité chimique, édition améliorée. Récupéré des livres.Google.co.aller
- « Caractéristiques de haute montagne, temps, faune, flore, emplacement
- Caractéristiques de l'art mésopotamien, peinture, sculpture, céramique »

