Solution hypertonique
- 967
- 231
- Lucas Schneider
Nous expliquons quelles sont les solutions hypertoniques, leurs caractéristiques, quelle est l'utilisation, les différences avec l'hypotonique et donnent plusieurs exemples
Beaucoup seront surpris de savoir que la façon dont les plantes absorbent l'eau à travers leurs racines et la façon dont les doigts des mains sont ridés lorsqu'ils se baignent dans l'eau de mer, ils sont étroitement liés.
Les deux choses se produisent grâce à l'existence d'une membrane qui fonctionne comme un filtre et une solution hypertonique qui suce littéralement de l'eau à travers. Mais qu'est-ce qu'une solution hypertonique?
Dans cet article, cette question sera répondue, et les caractéristiques les plus pertinentes des solutions hypertoniques seront également présentées, à quoi ils servent, comment ils se distinguent des autres types de solutions et quelques exemples de la même chose.
Qu'est-ce qu'une solution hypertonique?
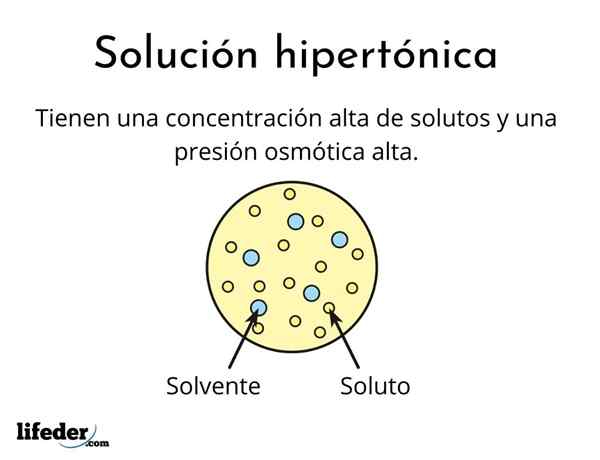
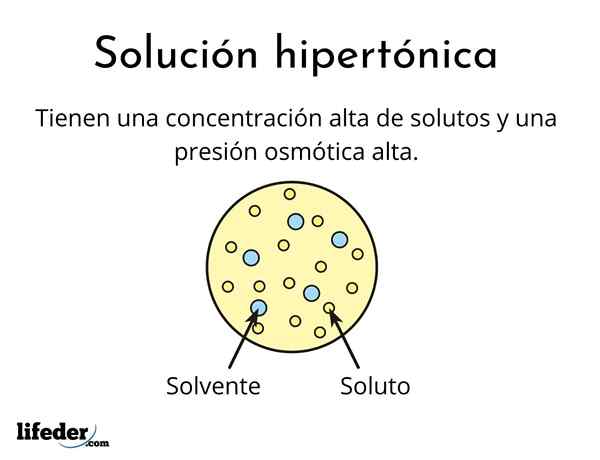
Ongle solution hypertonique C'est celui qui contient une concentration totale de solutés actifs osmolaires supérieurs à celui d'une autre solution de référence. Osmolly actif signifie que les solutés ne peuvent pas traverser un type spécial de membrane (similaire à un tissu) qui agit comme une crépine ou un filtre, c'est-à-dire que l'eau passer, et non aux particules de soluté.
Cette concentration élevée de solutés fait que les solutions hypertoniques ont une pression osmotique élevée. Cette pression est ce qui aspire pratiquement l'eau à travers la membrane, qui est appelée osmose.
Le mot hypertonique vient du préfixe grec hyper-, qui signifie "sur ou au-dessus" et "tons", ce qui signifie la tension ou la pression, donc hypertonique signifie littéralement "qu'il a une plus grande pression ou tension".
Il est important de garder à l'esprit que, en biologie et en médecine, à condition qu'il y ait une solution hypertonique, il se réfère à une solution plus concentrée que la solution contenue dans le sang, qui est appelée plasma sanguin.
Caractéristiques des solutions hypertoniques
Les solutions hypertoniques ont des caractéristiques de base:
Ils sont formés par un solvant et au moins un soluté
Aucune solution ne peut être hypertonique, même si elle est très concentrée. Le soluté doit être incapable de traverser la membrane, tandis que l'eau doit être capable de la passer sans problème, sinon, la pression osmotique n'est pas générée.
Ils ont des concentrations élevées de solutés
C'est ce qui en fait des solutions hypertoniques. Comme mentionné il y a un instant, les solutions hypertoniques sont plus concentrées que le sang.
Il peut vous servir: distillation fractionnée: processus, équipement, applications, exemplesIls peuvent avoir différentes compositions
Une solution hypertonique peut contenir un seul soluté comme le sel, ou peut contenir un mélange de solutés tels que les sels et les sucres, par exemple.
Les solutos peuvent être ioniques, neutres ou les deux
Les ventes contiennent des ions avec des frais électriques qui ne les laissent pas traverser la membrane, donc ils sont petits. D'autres solutés n'ont pas d'ions, mais ils sont grands et grasses et ne passent pas à travers les trous.
Ils ont une pression osmotique élevée
Comme mentionné ci-dessus, les solutions hypertoniques ont une pression osmotique supérieure à celle du sang.
Ils peuvent déshydrater les cellules
Des solutions hypertoniques extraient l'eau des cellules les laissant comme des raisins secs. C'est pourquoi nos mains et nos pieds sont ridés lorsque nous nous baignons sur la plage.
Quelles sont les solutions hypertoniques pour?
Les solutions hypertoniques ont de nombreuses utilisations dans la vie quotidienne, et aussi en médecine. Certaines des utilisations les plus courantes sont:
Ils sont utilisés pour garder la nourriture
- Exemple: les pêches dans le sirop ne pourrissent pas car le sirop a beaucoup de sucre dissous et est une solution très hypertonique. En déshydratant les cellules, les solutions hypertoniques ne permettent pas aux champignons et aux bactéries dans la nourriture, car elles meurent de soif. Cela permet aux aliments de durer plus.
Ils servent à réduire l'inflammation
- Exemple: lorsque quelqu'un a un accident et frappe la tête, il y a de nombreuses fois une inflammation dans le cerveau. Pour guérir le patient, les médecins injectent une solution de solution saline à 7,5%. Cette solution suce pratiquement l'eau, réduisant l'inflammation dans le cerveau.
Ils servent à remplacer les électrolytes.
- Exemple: le sodium est un électrolyte que nous devons vivre, et lorsqu'un patient a peu de sodium dans le sang, une solution saline à 7,5% est injectée pour reconstituer le sodium qui a été perdu.
Ils sont utilisés pour la nourriture parentérale
- Exemple: lorsque les gens ne peuvent pas manger par la bouche ou par un tube, ils se nourrissent d'une solution hypertonique qui contient un type de sucre appelé glucose.
Différences avec les solutions hypotoniques et isotoniques
Tout comme il existe des solutions hypertoniques, il existe également des solutions hypotoniques et isotoniques. La différence entre ces dernières et les solutions hypertoniques est sa concentration. Les solutions hypotoniques sont celles qui sont moins concentrées que le sang, et les isotoniques ont la même concentration que le sang.
Par exemple, l'eau pure, car elle n'a rien de soluté, est hypotonique, tandis que l'eau de coco a des sels et des sucres avec une concentration presque égale à celle du sang, il est donc isotonique.
En plus de la différenciation par leur concentration, les solutions hyper, hypo et isotoniques diffèrent dans la façon dont ils affectent les cellules.
L'image suivante montre l'effet des différents types de solutions sur les globules rouges (les petites cellules qui rendent le sang rouge).
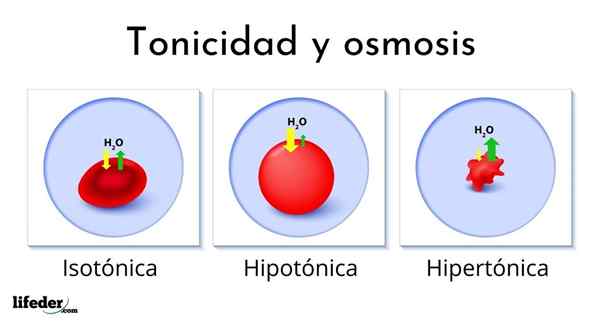
Si les globules rouges sont introduits dans une solution hypertonique, il extrait l'eau, les déshydratants et les laissant ridés comme une passe.
D'un autre côté, s'ils sont introduits dans une solution hypotonique, les globules rouges absorbent l'eau et gonflent, même en éclatement comme un ballon qui gonfle trop. Enfin, s'ils sont introduits dans une solution isotonique, l'eau à l'intérieur et à l'extérieur des globules rouges sera en équilibre, donc rien ne se passe.
Exemples de solutions hypertoniques
Sirop de sucre
 Pêches dans le sirop
Pêches dans le sirop Le sirop dans lequel les pêches et autres fruits sont préservés contient des concentrations de sucre très élevées, c'est donc une solution hypertonique.
La saumure
La saumure est une solution d'eau et de sel avec des concentrations très élevées comprises entre 3,5% et 25%, ce qui peut devenir près de 30 fois plus concentré que le sang (c'est-à-dire qu'il est très hypertonique).
Le vinaigre
Un vinaigre commun est une solution hypertonique, car elle a une concentration entre 3% et 5% d'acide acétique. Les réductions de vinaigre balsamique sont encore plus concentrées.
Peut vous servir: diméthylamine ((CH3) 2NH): structure, propriétés, utilisations, risquesLe même sang de nos veines, après avoir beaucoup transpiré.
Lors de l'exercice et de la transpiration, le corps élimine l'eau et les sels, mais élimine plus d'eau que les sels (la sueur est hypotonique) afin que le sang se concentre et devient hypertonique.
Eau de mer
L'eau de mer contient de nombreux sels dissous, avec une concentration totale d'environ 3,5%, ce qui le rend hypertonique. C'est pourquoi l'eau de mer ride nos doigts.
Boissons sucrées
Les boissons au cola et autres boissons sucrées peuvent contenir jusqu'à 10% de sucre, ainsi que les sels et autres solutés avec des concentrations supérieures au sang.
Solution de dextrose à 5% et 0,45% de chlorure de sodium (D5 ½ ns)
Ceci est un exemple de solution hypertonique qui est utilisée pour nourrir les personnes qui ne peuvent normalement pas manger par la bouche.
25% de mannitol
Ceci est une solution fréquemment utilisée pour traiter les chocs sur la tête. Il est quatre fois plus concentré que le sang.
Solution saline à 7,5%
Il s'agit d'une solution saline assez concentrée qui est également injectée avec certains patients atteints de certaines maladies dans les veines.
Jus commerciaux
Tous les jus achetés dans le supermarché et qui ne sont pas naturels, ont des concentrations de sucre très élevées qui les rendent hypertoniques.
Les références
- Sweeney J. Gérer l'hypernatrémie. Allaitement. Septembre 2010; 40 (9): 63.
- Eau salée. Wikipédia. 2021. Pris à partir de.Wikipédia.org / wiki / saumure.
- Eau de mer. Wikipédia. 2021. Pris à partir de.Wikipédia.Org / wiki / eau de mer.
- Chavaltamrong B, Pidatcha P, Thavisri U. Électrolytes, sucre, calories, osmolarité et pH des boissons et de l'eau de coco. Asie du Sud-Est J Trop Med Santé publique. Septembre 1982; 13 (3): 427-431.
- 5% de dextrose et 0.45% d'injection de chlorure de sodium, USP. FDA. 2006. Pris sur AccessData.FDA.Gov / Drugsatfda_Docs / Label / 2006/017607S123LBL.Pdf.
- Llorente G, Niño MC. Manitol contre solution saline hypertonique en neuroanesthésie. Magazine Colombien Anesthesiology. Janvier-mars 2015; 43 (1): 29-39.
- Saints mm, e. Traitement de l'acidose lactique du rumen aigu avec des solutions intraveineuses de chlorure de sodium hypertonique ou de bicarbonate baisée par l'eau intrauminale. Recherche en science vétérinaire. Février 2020; 128: 24-34.
- Dini-g. E, Abreu-C. JD, López-M. ET. Osmolalité des boissons de consommation fréquentes. Recherche clinique. Décembre 2004; 45 (4).

