Structure d'hydrazine, propriétés, synthèse, utilisations

- 1445
- 234
- Raphaël Meyer
La Hydrazine C'est un composé inorganique dont la formule chimique est n2H4. Il se compose d'un membre de la famille des hydrors d'azote, le plus simple étant le plus simple d'être. Bien que sa molécule apparaisse à la simplicité, elle présente plusieurs propriétés chimiques et physiques qui font de l'hydrazine une substance intéressante et énergiquement prometteuse.
Gardez une similitude étroite avec l'eau, car les deux existent en tant que substances liquides dans des intervalles de températures similaires. De l'hydrazine, nous pouvons obtenir des dérivés organiques en remplaçant ses hydrogènes par des groupes gazéifiés. Aussi, à partir de celui-ci, des hydrazons, des hydrazides et des sels d'hydrazine sont synthétisés.
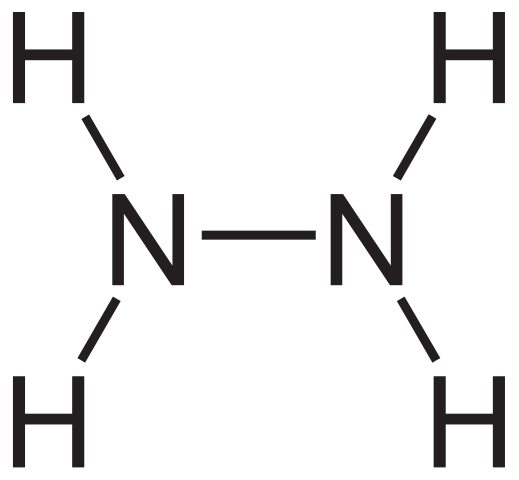 Formule structurelle hydrazine. Source: Neurotoger via Wikipedia.
Formule structurelle hydrazine. Source: Neurotoger via Wikipedia. La formule structurelle de l'hydrazine peut être vue ci-dessus, qui peut être écrite comme h2NNH2 ou h2N-nh2. Si vous regardez attentivement, il semble que deux molécules NH3 Ils se seraient liés les uns aux autres. Cependant, dans la formation du lien N-N, non seulement les molécules d'ammoniac comme réactifs sont impliqués.
L'hydrazine est un composé qui a plusieurs applications, car il s'agit d'un excellent précurseur pour les symphines de composés, à la fois organiques et inorganiques. De même, grâce à sa puissance de réduction et à ses produits de décomposition, il est destiné à éliminer l'oxygène et d'autres gaz, obtenir des métaux précieux; Et surtout, pour stimuler les vaisseaux spatiaux et l'état de l'avion -art.
[TOC]
Structure hydracine
Molécule et lien
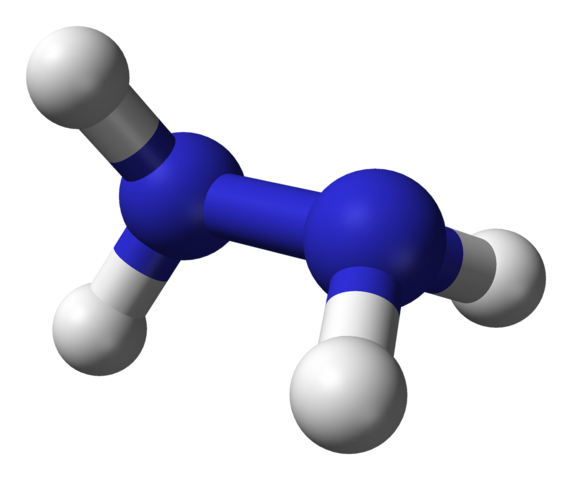 Structure moléculaire de l'hydrazine. Source: Ben Mills via Wikipedia.
Structure moléculaire de l'hydrazine. Source: Ben Mills via Wikipedia. Dans l'image supérieure, nous avons la molécule d'hydrazine représentée par un modèle de sphères et de barres. Notez que l'orientation spatiale des atomes d'hydrogène, sphères blanches, contraste avec l'impression offerte par la formule structurelle; c'est-à-dire les hydrogènes des deux -NH2 Ils ne sont pas alignés ou éclipsés, mais ont un angle de rotation à 95 °.
En fait, c'est tellement que la liaison N-N est à peine capable de tourner, ayant une barrière d'énergie qui doit être expirée pour éclipser les quatre atomes d'hydrogène.
Ca parle de quoi? En principe, à de fortes répulsions électroniques qui éprouvent mutuellement les deux paires d'électrons solitaires sur les atomes d'azote. Cet angle à 95 ° est celui qui donne à la molécule d'hydrazine la plus grande stabilité.
Peut vous servir: Bromide au lithium: structure, propriétés, utilisations, risquesGéométries
Chaque atome d'azote a une hybridation SP3, Adopter une géométrie pyramide triangulaire. Par conséquent, avec les paires d'électrons libres, la molécule de l'hydracine telle que deux pyramides liées par l'un de ses sommets pourrait être visualisée et dans les centres duquel les atomes d'azote seraient situés.
Interactions intermoléculaires
La formule H2NNH2 Je pourrais donner la fausse idée que l'hydrazine est un composé apolaire pour avoir deux groupes égaux liés. Cependant, la structure moléculaire et sa liaison N-N tournée montrent que la molécule n'est pas complètement symétrique, mentionnant également que leurs paires d'électrons libres ne pointent pas dans les directions contraires.
Cela signifie que l'hydrazine, étant structurellement et électroniquement asymétrique, présente un moment dipolaire. Et par conséquent, leurs molécules interagissent entre elles par dipole-dipol2NNH2-NH2NH2, qui sont responsables de l'hydrazine ayant un point d'ébullition très élevé.
Propriétés de l'hydracine
 Hydrazine hydraté. Source: lhchem / cc by-sa (https: // CreativeCommons.Org / licences / by-sa / 3.0)
Hydrazine hydraté. Source: lhchem / cc by-sa (https: // CreativeCommons.Org / licences / by-sa / 3.0) Apparence physique
L'hydrazine est un liquide incolore similaire à l'eau en ce qui concerne la viscosité et la densité. Lors de la brûlure, il émet des vapeurs blanches, en plus de gagner de l'ammoniac et du poisson.
Masse molaire
32.0452 g / mol
Point de fusion
2 ºC.
Point d'ébullition
114 ºC. Notez que l'hydrazine existe à l'état liquide dans l'intervalle de température 2-114 ºC, très similaire à celui de l'eau, 0-100 ºC.
Densité
1.021 g / cm3
Densité de vapeur
1.1 dans la relation aérienne.
La pression de vapeur
Environ 0.010 atm à 30.7 ºC
Solubilité
L'hydrazine est miscible avec de l'eau, ainsi qu'avec plusieurs alcools primaires. L'hydrazine forme un hydrate avec de l'eau, n2H4· H2Ou, caractérisé par le fait d'être plus dense que l'hydrazine pure ou anhydre. Cet hydrate est le produit le plus commercialisé, car il est plus stable et bon marché.
Moment dipolaire
1.85 D. C'est une substance plutôt polaire, presque la même que l'eau.
Il peut vous servir: acide yodium (HIO3): structure, propriétés, risques et utilisationsGelée
0.876 CP
point de rupture
52 ºC
Température d'auto-direction
Varie en fonction des substances ou des surfaces avec lesquelles il entre en contact. Par exemple, sur les oxydes de fer brûle à 23 ° C, tandis que sur du verre ou d'autres récipients, il ne commence pas à être enflammé avant 270 ºC.
Décomposition
Lorsqu'il brûle dans l'air, il se décompose en oxydes d'azote, nonX. Mais en ce qui concerne sa décomposition catalytique, c'est-à-dire que celle accélérée par des oxydes métalliques ou des métaux, des produits tels que l'ammoniac, l'azote et l'hydrogène sont obtenus, et une immense quantité de chaleur, qui finit par former une flamme brûlante mais invisible.
Réactivité
L'hydrazine est un bon agent réducteur, car lorsque l'oxydé produit de l'eau et de l'azote, les deux composés qui ne souffrent pas de réactions secondaires.
D'un autre côté, l'hydrazine est un nucléophile, car il utilise ses paires d'électrons libres pour rejoindre d'autres molécules organiques. De même, il peut souffrir de remplacement3, Pour produire des dérivés méthylés: ch3NHNH2 ou (ch3)2NNH2.
Réagit avec des acides forts pour former des sels d'hidrazinio, n2H5X, et de Hidrazonio, n2H6X2. Ces derniers sont les moins courants. Sulfate d'hydrazinium, [n2H5] HSO4, Il est préparé en réagissant à l'hydrate d'hydrazine avec de l'acide sulfurique.
Basicité
L'hydrazine est une base plus faible que l'ammoniac:
N2H4(AC) + H2Ou (l) ⇌ n2H5+(Ac) + oh-(AC)
Kb = 1.3 · 10-6
En effet, l'acide conjugué à l'hydrazinio2H5+ ou h3N+-NH2, a sa charge déstabilisée par l'effet d'attracteur du groupe NH2; c'est-à-dire qu'au lieu de fournir une densité électronique à l'azote positif, le retrait.
L'hydrazine est capable de souffrir d'une seconde protonation, beaucoup moins probable, qui génère un acide conjugué encore plus instable:
N2H5+(AC) + H2Ou (l) ⇌ n2H6+(Ac) + oh-(AC)
Kb = 8.4 · 10-16
L'hydrazonium, n2H6+ ou h3N+-N+H3, Il est très instable en raison des répulsions entre les charges positives des deux atomes d'azote. Cependant, en compagnie de certains anions, elle peut exister en tant que sel.
Toxicité
L'anhydra hydrazine est une substance extrêmement toxique, caustique et peut-être cancérigène, sans oublier qu'elle est très explosive, elle ne devrait donc être manipulée que sous des protocoles de sécurité stricts.
Peut vous servir: facteur de compressibilité: comment calculer, exemples et exercicesLa synthèse
La méthode la plus utilisée pour synthétiser l'hydrazine est le processus Raschig. Cela se compose des deux réactions suivantes:
NH3(AC) + NaOCl (AC) → NH2Cl (ac) + NaOH (AC)
2nh3(AC) + NH2Cl (ac) → n2H4(AC) + NH4Cl (AC)
À la fin, l'hydrate N est formé2H4· H2Ou, qui est distillé en présence de KOH ou NaOH sous forme de solides secs:
N2H4· H2O → N2H4
De cette façon, l'anhydra hydrazine est obtenue et la liaison N-N est formée.
Hydrazine utilise
 L'hydrazine est l'une des substances les plus appréciées du boom aérospatial. Source: pxhere.
L'hydrazine est l'une des substances les plus appréciées du boom aérospatial. Source: pxhere. - L'hydrazine, en présence de catalyseurs métalliques, est décomposé de manière exolémique pour produire de l'azote et de l'hydrogène, fournissant ainsi suffisamment d'énergie pour stimuler les avions, les roquettes et les satellites.
- Cette tendance à se décomposer et à provoquer des gaz est utilisée avec précision pour gonfler les matériaux polymères, tels que le caoutchouc ou le polyéthylène, les transformant en leurs mousses respectives.
- De même, en libérant des gaz, ceux-ci peuvent traîner d'autres qui sont dissous dans les tuyaux des tuyaux, il est donc très utile d'éliminer l'oxygène des chaudières, évitant ainsi qu'ils se corrodent.
- L'hydrazine est un matériau précurseur pour de nombreux composés organiques avec des fonctions pharmacologiques, des antifungicides, des herbicides, des insecticides, des engrais, etc. Cela en est dû à une grande variété de dérivés cycliques d'azote sont synthétisés.
- Enfin, étant un bon agent réducteur, l'hydrazine et ses sels d'hydrazinium sont utilisés pour réduire les minéraux métalliques précieux, étant d'une grande valeur dans l'industrie métallurgique.
Les références
- Fhiver & Atkins. (2008). Chimie inorganique. (Quatrième édition). Mc Graw Hill.
- Wikipédia. (2020). Hydrazine. Récupéré de: dans.Wikipédia.org
- Centre national d'information sur la biotechnologie. (2020). Hydrazine. PubChem Comunund Résumé pour CID 9321. Récupéré de: pubchem.NCBI.NLM.NIH.Gouvernement
- Les éditeurs d'Enyclopaedia Britannica. (2020). Hydrazine. Britannica Encyclopaedia. Récupéré de: Britannica.com
- Iridium Suivant. (20 juin 2017). Hydrazine - toxique pour les humains, mais les satellites l'adorent. Récupéré de: iridium.com
- « Les 95 meilleures phrases de The Walking Dead
- Causes d'indépendance du bassin, développement, conséquences »

