Structure de diméthylanylin, propriétés, synthèse, utilisations
- 1594
- 147
- Raphaël Charles
La diméthylanylin O dimétilphényllamine est un composé organique formé par un anneau de benzène avec un groupe amino remplacé par deux groupes méthyliques. Sa formule chimique est C8HonzeN.
Il est également connu sous le nom de n, n-diméthylanylane, car il s'agit d'un dérivé de toute ligne dans laquelle les hydrogènes du groupe amino sont remplacés par deux groupes méthyle. Cela en fait une amine tertiaire.
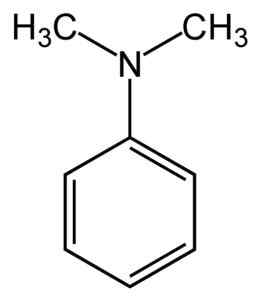 Structure de n, n-diméthylanylin. Aucun auteur lisible par machine fourni. MySid a supposé (sur la base des réclamations du droit d'auteur). [CC BY-SA 3.0 (http: // CreativeCommons.Org / licences / by-sa / 3.0 /]]. Source: Wikipedia Commons.
Structure de n, n-diméthylanylin. Aucun auteur lisible par machine fourni. MySid a supposé (sur la base des réclamations du droit d'auteur). [CC BY-SA 3.0 (http: // CreativeCommons.Org / licences / by-sa / 3.0 /]]. Source: Wikipedia Commons. N, n-diméthylanylin est un liquide huileux jaune pâle à brun avec l'odeur caractéristique des amines. C'est un composé de base et réagit avec l'acide nitreux formant un nitrosocompose. Lorsqu'il est exposé à l'air, il devient brun.
Il est utilisé dans la fabrication de colorants pour les peintures. Il est également utilisé comme activateur des catalyseurs de polymérisation et dans des mélanges utilisés pour l'enregistrement d'images. À son tour, il a été utilisé dans la synthèse de composés ou d'antibiotiques antibactériens comme certaines céphalosporines dérivées de la pénicilline. N, N-diméthyananylin est également une base pour obtenir d'autres composés chimiques.
C'est un liquide combustible et lorsqu'il est chauffé jusqu'à la décomposition émet des vapeurs toxiques. L'exposition aiguë de l'être humain au N, le N-diméthyanyanylin peut entraîner des effets négatifs tels que les maux de tête, les étourdissements, la diminution de l'oxygène sanguin et la coloration de la peau bleuâtre, entre autres symptômes.
[TOC]
Structure
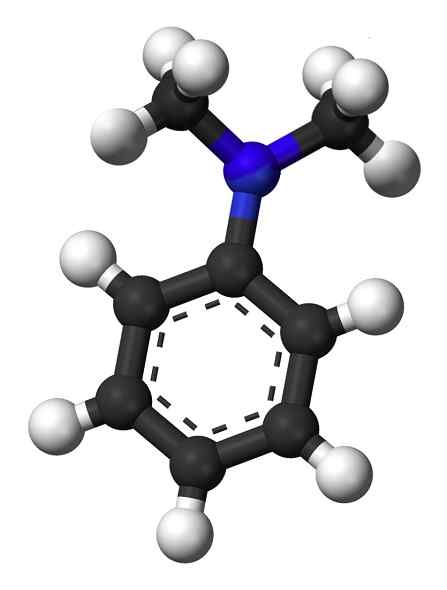
La figure suivante montre la structure spatiale du n, n-diméthylanylinaire:
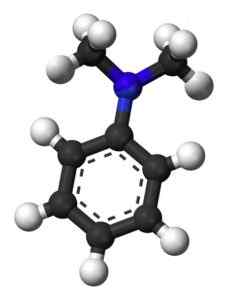 Structure spatiale du n, n-diméthylanylin. Esquilo [domaine public]. Source: Wikipedia Commons.
Structure spatiale du n, n-diméthylanylin. Esquilo [domaine public]. Source: Wikipedia Commons. Nomenclature
- N, n-diméthylanylin
- Diméthylanylin
- Diméthylphényllamine
- N, n-diméthyl bencenamine
N est placé dans le nom pour indiquer que les deux groupes méthyle (-ch3) sont attachés à l'azote (n) et non à la bague Benncénico.
Propriétés
État physique
Liquide pâle à brun.
Poids moléculaire
121.18 g / mol.
Peut vous servir: anion: formation, caractéristiques et typesPoint de fusion
3 ºC.
Point d'ébullition
194 ºC.
Point d'inflammation
63 ºC (méthode de coupe fermée). C'est la température minimale à laquelle les vapeurs peuvent être activées si une flamme y est transmise.
La pression de vapeur
0,70 mm Hg à 25 ºC.
Température d'auto-direction
371 ºC. Il s'agit de la température minimale à la pression atmosphérique spontanée, sans source externe de chaleur ou de flamme.
Densité
0,9537 g / cm3 à 20 ºC.
Indice de réfraction
1 5582 à 20 ºC.
Solubilité
Dans l'eau, il est très peu soluble: 1 454 mg / L a 25 ºC.
Librement soluble dans l'alcool, le chloroforme et l'éther. Soluble dans l'acétone, le benzène et les solvants oxygénés et chlorés.
Constante de basicité
Kb 11.7, qui indique la facilité avec laquelle ce composé accepte un ion hydrogène de l'eau.
Propriétés chimiques
N, n-diméthylanylin est un composé de base. Réagit avec l'acide acétique pour donner de l'acétate de n, n-dimétianilinio.
Le groupe -n (choisissez3)2 du n, n-diméthyananylin est un puissant activateur de substitution aromatique en position pour de l'anneau de benzène.
Réagit avec du nitrite de sodium (nano2) En présence d'acide chlorhydrique (HCL) formant P-nitroso-n, n-diméthylanylin. Aussi avec l'acide nitreux génère le même composé nitrosado en position pour.
Lors de la réaction du n, n-dimélaniline avec le chlorure de benzononium, dans un milieu doucement acide, il y a un type Azocomposé AR-N = n-ar ', où AR est un groupe aromatique. Les molécules avec des groupes azo sont des composés fortement colorés.
Des risques
Lorsqu'il est chauffé à sa décomposition émet des vapeurs très toxiques d'oxydes d'azote nonX.
C'est un liquide combustible.
Il se décompose lentement dans l'eau exposée au soleil. Il n'est pas biodégradé.
Il est volatilisé des surfaces de sol humide et d'eau. N'évaporez pas le sol sec et passez à travers cela. Ne s'accumule pas dans les poissons.
Peut vous servir: Sulfure de fer (II): propriétés, risques et utilisationsPeut être absorbé par la peau. Il est également rapidement absorbé par l'inhalation. L'exposition de l'être humain à N, n-diméthyananylin peut diminuer la teneur en oxygène du sang entraînant une couleur de peau bleuâtre.
L'inhalation aiguë de ce composé peut entraîner des effets négatifs pour le système nerveux central et le système circulatoire, avec des maux de tête, de la cyanose et des étourdissements.
La synthèse
Cela peut se produire de plusieurs manières:
- De l'aniline et du méthanol sous pression en présence de catalyseurs acides, tels que H2Swin4. Le sulfate est obtenu, qui devient la base en ajoutant de l'hydroxyde de sodium.
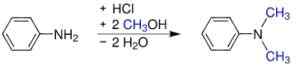 S synthèse, n-diméthylanylin. Werderkli - propre travail. Domaine public. Source: Wikipedia Commons.
S synthèse, n-diméthylanylin. Werderkli - propre travail. Domaine public. Source: Wikipedia Commons. - Passer une vapeur d'aniline et un éther diméthylique sur l'oxyde d'aluminium activé.
- Chauffer un mélange d'aniline, de chlorure d'anilinium et de méthanol sous pression puis de distillation.
Applications
Dans l'industrie des colorants
Pour la propriété de réagir avec le chlorure de bencodiazonium formant des azocompiestos, le n-diméthylanylin est utilisé comme intermédiaire dans la fabrication de colorants.
C'est la matière première dans la synthèse des colorants de la famille de méthyl violet.
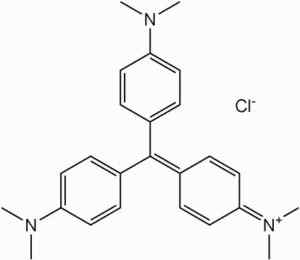 Coloriage de méthyl violet. Aucun auteur lisible par machine fourni. Shaddack supposé (basé sur les réclamations du droit d'auteur). [Domaine public]. Source: Wikipedia Commons
Coloriage de méthyl violet. Aucun auteur lisible par machine fourni. Shaddack supposé (basé sur les réclamations du droit d'auteur). [Domaine public]. Source: Wikipedia Commons Dans la fabrication de mélanges photocurables
Le n, n-diméthyananylin fait partie d'un mélange photocurable qui subit la réaction de guérison à la suite d'une sensibilité élevée à la lumière visible ou à la fermeture infrarouge, afin qu'elle puisse être utilisée pour enregistrer des images ou des matériaux photoorestonants.
N, n-diméthyananylin est l'un des composants du mélange qui provoquent la conscience des longueurs d'onde, de sorte que la composition est guéris avec une lumière d'onde à faible énergie.
Il peut vous servir: dérivés de benzèneOn estime que la fonction du n, n-diméthylanyanylin est probablement pour supprimer la réaction de terminaison de la polymérisation radicale causée par l'oxygène.
Dans la fabrication en fibre de verre
N, n-diméthylanylin est utilisé comme serre-serre catalytique dans certaines résines en fibre de verre.
Dans la synthèse des antibiotiques
N, N-diméthylanylin participe à la synthèse des céphalosporines basées sur des pénicillines.
Les sulfoxydes de pénicilline sont convertis en CEFEMES lorsqu'ils sont chauffés en présence de catalyseurs de base tels que N, N-diméthylanylin.
Ces céphalosporines présentent une activité antibactérienne contre les organismes Gram positifs et Gram-négatifs, ainsi que contre les staphylocoques résistants à la pénicilline.
 Antibiotiques. Alina Kuptsova. Source: Pixabay.
Antibiotiques. Alina Kuptsova. Source: Pixabay. Cependant, il convient de noter que N, N-diméthylanylanne reste dans ces antibiotiques comme impureté.
Sur les réactions chimiques
N, N-diméthylanylin est utilisé dans l'activation des catalyseurs de polymérisation des oléfines.
Il est utilisé avec le pentafluorophénol (C6F5Oh) avec qui forme le composé ionique [hnphme2]]+[H (OC6F5)2]]-. Ce composé ionique a un ou deux protons actifs qui activent le catalyseur basé sur un métal de transition.
De plus, dans la fabrication de résines, le n-diméthylanylin a été utilisé comme accélérateur de polymérisation ou promoteur pour les résines en polyester. Son action génère un durcissement rapide de la résine.
Dans plusieurs applications
Il est utilisé dans la synthèse d'autres composés chimiques, par exemple, la vanilline et comme intermédiaire pour les médicaments pharmaceutiques.
Il est également utilisé comme solvant, comme agent alkylant, comme stabilisateur et pour fabriquer des peintures et des revêtements.
Les références
- S. Bibliothèque nationale de médecine. (2019). N, n-diméthylaniline. Récupéré de: pubchem.NCBI.NLM.NIH.Gouvernement
- Morrison, R.T. Et Boyd, R.N. (2002). Chimie organique. 6e édition. Prentice Hall.
- (2000). N, n-diméthylaniline. Résumé. Récupéré de l'EPA.Gouvernement
- Zanaboni, P. (1966). Composition résineuse de polyester insaturée Havh Stabilité et durcissement rapide à basse température en utilisant un mélange de diméthylanil, de trenhanolamine et de diphénylamine. OU.S. Brevet non. 3 236 915. 22 février 1966.
- Nudelman, un. et McCaully, R.J. (1977). Processus pour le réarrangement des pénicillines aux céphalosporines et aux composants intermédiaires de ceux-ci. OU.S. Brevet non. 4 010 156. 1er mars 1977.
- Kouji Inaishi (2001). Composition photocurable. OU.S. Brevet non. 6 171 759 B1. 9 janvier 2001.
- Luo, L. et al. (2012). Acide ionique. OU.S. Brevet non. 8 088 952 B2. 3 janvier 2012.
- « Historique, propriétés, structure, utilisations, risques de Rodio
- Caractéristiques et exemples des sons aigus »

