Darmstadtio Discovery, Structure, propriétés, utilisations

- 2107
- 331
- Raphaël Charles
Il Darmstadtio Il s'agit d'un élément chimique ultra lourd situé dans la série transactinide, qui commence juste après le métal Lawrencio. C'est spécifiquement dans les groupes 10 et 7 du tableau périodique, étant les congénères des métaux nickel, paladium et platine.
Il a un symbole chimique, avec un nombre atomique de 110, et ses très peu d'atomes qui se sont synthétisés sont pratiquement décomposés instantanément. C'est donc un élément éphémère. Synthétiser et détecter qu'il représentait un exploit dans les années 90 du siècle dernier, prenant le crédit de sa découverte un groupe de chercheurs allemands.
 L'élément Darmstadtio a été découvert à l'Institut allemand GSI, dans la ville de Darmstadt. Source: Commandant-Pirx chez allemand wikipedia [cc by-s (https: // CreativeCommons.Org / licences / by-sa / 3.0)]
L'élément Darmstadtio a été découvert à l'Institut allemand GSI, dans la ville de Darmstadt. Source: Commandant-Pirx chez allemand wikipedia [cc by-s (https: // CreativeCommons.Org / licences / by-sa / 3.0)] Avant sa découverte et qu'il a été discuté de ce que devrait être son nom, le système de nomenclature IUPAC avait officiellement nommé «Unaunilio», qui signifie «un seul zéro», égal à 110. Et plus loin derrière cette nomenclature, selon le système Mendeleev, son nom était EKA-Platino pour penser chimiquement à ce métal.
Darmstadtio est un élément non seulement éphémère et instable, mais aussi hautement radioactif, dans les désintégrations nucléaires de laquelle la plupart de ses isotopes libèrent des particules alfas; Ce sont des noyaux nus d'hélio.
En raison de sa vie éphémère, toutes ses propriétés sont estimées et ne peuvent jamais être utilisées dans un but particulier.
[TOC]
Découverte
Mérite allemand
Le problème autour de la découverte de Darmstadtio était que plusieurs équipes de chercheurs se sont consacrées à leur synthèse au cours des années successives. Dès que son atome s'est formé, il s'estompa dans des particules irradiées.
Par conséquent, il ne pouvait pas tâtonner lequel des équipes méritait le crédit d'avoir synthétisé d'abord, lorsqu'il le détectait même représentait déjà un défi, déclinant si rapidement et libérant des produits radioactifs.
Il peut vous servir: acide tanique: structure, propriétés, obtention, utilisationsDans la synthèse de Darmstadtio, ils ont travaillé par des équipes distinctes des centres d'investigation suivants: Central Institute of Nuclear Research à Dubná (d'ici là l'Union soviétique), Lawrence Berkeley National Laboratory (États-Unis) et le Centre de recherche lourde (abrégé en allemand en tant que GSI GSI ).
Le GSI est situé dans la ville allemande de Darmstadt, où en novembre 1994, ils ont synthétisé l'isotope radioactif 269Ds. Les autres équipes ont synthétisé d'autres isotopes: 267Ds dans l'icin, et 273DS dans le LNLB; Cependant, ses résultats n'avaient pas été concluants aux yeux critiques de l'IUPAC.
Chaque équipe avait proposé un nom particulier pour ce nouvel élément: Hahnio (ICIN) et Bequerelio (LNLB). Mais après un rapport de l'IUPAC en 2001, l'équipe allemande GSI avait le droit de nommer l'élément darmstadtio.
La synthèse
Darmstadtio est un produit de la fusion des atomes métalliques. Qui? En principe, un relativement lourd qui sert de blanc ou de cible, et une autre lumière qui sera entrée en collision contre la première à une vitesse égale au dixième de la vitesse de la lumière dans un vide; sinon, les répulsions entre ses deux noyaux n'ont pas pu être surmontées.
Une fois que les deux noyaux sont entrés en collision efficacement, une réaction de fusion nucléaire se produira. Les protons se joignent, mais le sort des neutrons est différent. Par exemple, le GSI a développé la réaction nucléaire suivante, dont le premier atome s'est produit 269DS:
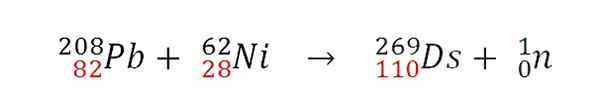 Réaction nucléaire pour la synthèse d'un atome isotope 269DS. Source: Gabriel Bolívar.
Réaction nucléaire pour la synthèse d'un atome isotope 269DS. Source: Gabriel Bolívar. Notez que les protons (en rouge) sont ajoutés. Variant les masses atomiques des atomes colladés, différents isotopes de Darmstadtio sont obtenus. En fait, le GSI a fait des expériences avec l'isotope 64Au lieu de 62Non pas non plus ceux qui ne synthétisent que 9 atomes de l'isotope 271Ds.
Peut vous servir: aldéhydosLe GSI a réussi à créer 3 atomes de 269DS, mais après avoir exécuté trois billions de bombardement par seconde pour une semaine complète. Ces données offrent une perspective écrasante des dimensions de ces expériences.
Structure Darmstadtio
Parce que seul un atome de Darmstadtio par semaine peut être synthétisé ou créé, il est peu probable qu'il en ait assez pour établir un cristal; Sans oublier que l'isotope le plus stable est le 281Ds, dont t1/2 Ce n'est que 12,7 secondes.
Par conséquent, pour déterminer leur structure cristalline, les chercheurs sont basés sur des calculs et des estimations qui cherchent à aborder le panorama le plus réel. Ainsi, il a été estimé que la structure du Darmstadtio est centrée cubique sur le corps (BCC); Contrairement à ceux de leur nickel le plus léger, le paladium et les congénères de platine, avec des structures cubiques centrées sur les visages (FCC).
En théorie, les électrons les plus externes des Orbitals 6D et 7S doivent participer à leur lien métallique, selon leur configuration électronique estimée:
[RN] 5F146d87s2
Cependant, il est probablement connu expérimentalement à partir des propriétés physiques de ce métal.
Propriétés

Les autres propriétés de Darmstadtio sont également estimées, pour les mêmes raisons mentionnées pour sa structure. Cependant, certaines de ces estimations sont intéressantes. Par exemple, Darmstadtio serait un métal encore plus noble que l'or, ainsi que très dense (34,8 g / cm3) que l'osmium (22,59 g / cm3) et El Mercurio (13,6 g / cm3).
En ce qui concerne ses états d'oxydation possibles, il a été estimé qu'il serait +6 (DS6+), +4 (ds4+) et +2 (ds2+), égal à ceux de leurs pairs plus légers. Par conséquent, si les atomes de 281DS avant de se désintégrer, des composés tels que DSF seraient obtenus6 ou dscl4.
Il peut vous servir: 50 exemples d'acides et de basesÉtonnamment, il y a la probabilité de synthétiser ces composés, car 12,7 secondes, la t1/2 du 281DS, c'est plus que suffisant pour faire des réactions. Cependant, l'inconvénient continue d'être qu'avec juste un atome de ds par semaine, il est insuffisant pour collecter toutes les données requises par une analyse statistique.
Applications
Encore une fois, comme il s'agit d'un métal tellement rare, actuellement synthétisé en quantités atomiques et non massives, il n'y a pas de usage qui lui est réservé; Pas même dans un avenir lointain.
À moins qu'une méthode pour stabiliser ses isotopes radioactifs, les atomes de Darmstadtio ne seront utilisés que pour susciter la curiosité scientifique, en particulier en ce qui concerne la physique nucléaire et la chimie.
Mais si un moyen de les créer en quantités abondants est géré, plus de lumières seront jetées sur la chimie de cet élément ultra lourd et éphémère.
Les références
- Fhiver & Atkins. (2008). Chimie inorganique. (Quatrième édition). Mc Graw Hill.
- Wikipédia. (2020). Darmstadium. Récupéré de: dans.Wikipédia.org
- Steve Gagnon. (s.F.). L'élément darmstadium. Ressource de laboratoire de Jefferson. Récupéré de: éducation.Jlab.org
- Centre national d'information sur la biotechnologie. (2020). Darmstadium. Base de données PubChem. Récupéré de: pubchem.NCBI.NLM.NIH.Gouvernement
- Brian Clegg. (15 décembre 2019). Darmstadium. Chimie dans ses éléments. Récupéré de: Chemistryworld.com
- « Concept de numéro d'oxydation, comment le sortir et exemples
- Masse molaire comment il est calculé, exemples et exercices résolus »

